História da virologia

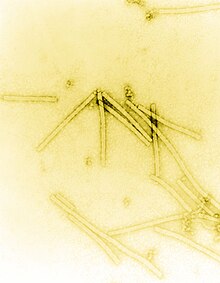
A história da virologia - o estudo científico dos vírus e das infecções que eles causam - começou nos últimos anos do século XIX. Embora Louis Pasteur e Edward Jenner tenham desenvolvido as primeiras vacinas para proteção contra infecções virais, eles não sabiam da existência de vírus.
A primeira evidência da existência de vírus veio de experimentos com filtros que tinham poros pequenos o suficiente para reter bactérias. Em 1892, Dmitri Ivanovsky usou um desses filtros para mostrar que a seiva de uma planta de tabaco doente permanecia infecciosa para as plantas de tabaco saudáveis, apesar de ter sido filtrada. Martinus Beijerinck chamou a substância infecciosa filtrada de "vírus" e essa descoberta é considerada o princípio da virologia.
A subsequente descoberta e caracterização parcial de bacteriófagos por Frederick Twort e Félix d'Herelle fortificou ainda mais o campo e, no início do século XX, muitos vírus foram descobertos. Em 1926, Thomas Milton Rivers definiu os vírus como parasitas obrigatórios. Wendell Meredith Stanley demonstrou que os vírus são partículas, em vez de um fluido, e a invenção do microscópio eletrônico em 1931 permitiu que suas estruturas complexas fossem visualizadas.
Pioneiros[editar | editar código-fonte]


Apesar de seus outros sucessos, Louis Pasteur (1822-1895) foi incapaz de encontrar um agente causador da raiva e especulou sobre um patógeno pequeno demais para ser detectado usando um microscópio.[1] Em 1884, o microbiologista francês Charles Chamberland (1851–1931) inventou um filtro - conhecido hoje como filtro de Chamberland - que tinha poros menores que bactérias. Assim, ele poderia passar uma solução contendo bactérias pelo filtro e removê-las completamente da solução.[2]
Em 1876, Adolf Mayer, que dirigia a Estação Experimental Agrícola em Wageningen, foi o primeiro a mostrar que o que chamou de "Doença do Mosaico do Tabaco" era infecciosa. Ele achava que a doença era causada por uma toxina ou uma bactéria muito pequena. Mais tarde, em 1892, o biólogo russo Dmitry Ivanovsky (1864–1920) usou um filtro de Chamberland para estudar o que hoje é conhecido como o vírus do mosaico do tabaco. Seus experimentos mostraram que extratos de folhas esmagadas de plantas de tabaco infectadas permanecem infecciosos após a filtração. Ivanovsky sugeriu que a infecção pode ser causada por uma toxina produzida por uma bactéria, mas não deu continuidade à ideia.[3]
Em 1898, o microbiologista holandês Martinus Beijerinck (1851–1931), professor de microbiologia da Escola Agrícola de Wageningen, repetiu os experimentos de Adolf Mayer e se convenceu de que o filtrado continha uma nova forma de agente infeccioso.[4] Ele observou que o agente se multiplicava apenas nas células em divisão e chamou-o de contagium vivum fluidum (germe vivo solúvel) e reintroduziu a palavra vírus.[3] Beijerinck sustentou que os vírus eram de natureza líquida, uma teoria mais tarde desacreditada pelo bioquímico e virologista norte-americano Wendell Meredith Stanley (1904-1971), que provou que eles eram de fato partículas.[3] No mesmo ano, 1898, Friedrich Loeffler (1852–1915) e Paul Frosch (1860–1928) passaram o primeiro vírus animal por um filtro semelhante e descobriram a causa da febre aftosa.[5]
O primeiro vírus humano a ser identificado foi o vírus da febre amarela.[6] Em 1881, Carlos Finlay (1833–1915), um médico cubano, primeiro conduziu e publicou uma pesquisa que indicava que os mosquitos carregavam a causa da febre amarela,[7] uma teoria comprovada em 1900 por uma comissão chefiada por Walter Reed (1851–1902). Durante 1901 e 1902, William Crawford Gorgas (1854–1920) organizou a destruição dos habitats de reprodução dos mosquitos em Cuba, o que reduziu drasticamente a prevalência da doença.[8] Posteriormente, Gorgas organizou a eliminação dos mosquitos do Panamá, o que permitiu a abertura do Canal[9] O vírus foi finalmente isolado por Max Theiler (1899–1972) em 1932, que desenvolveu uma vacina bem-sucedida.[10]
Não foi até a invenção do microscópio eletrônico em 1931 pelos engenheiros alemães Ernst Ruska (1906-1988) e Max Knoll (1887-1969),[11] que as partículas de vírus, especialmente os bacteriófagos, mostraram ter estruturas complexas. Os tamanhos dos vírus determinados usando este novo microscópio se encaixaram bem com aqueles estimados por experimentos de filtração. Esperava-se que os vírus fossem pequenos, mas a variedade de tamanhos foi uma surpresa. Alguns eram apenas um pouco menores do que as menores bactérias conhecidas, e os vírus menores eram de tamanhos semelhantes a moléculas orgânicas complexas.[12]
Em 1935, Wendell Stanley examinou o vírus do mosaico do tabaco e descobriu que era composto principalmente de proteína.[13] Em 1939, Stanley e Max Lauffer (1914) separaram o vírus em proteína e ácido nucléico,[14] que foi mostrado pelo colega de pós-doutorado de Stanley, Hubert S. Loring, ser especificamente RNA.[15] A descoberta do RNA nas partículas foi importante porque em 1928 Fred Griffith (c.1879–1941) forneceu a primeira evidência de que seu semelhante, o DNA, formava genes.[16]
Bacteriófagos[editar | editar código-fonte]

Descoberta[editar | editar código-fonte]
Os bacteriófagos são os vírus que infectam e se replicam nas bactérias. Eles foram descobertos no início do século 20, pelo bacteriologista inglês Frederick Twort (1877–1950).[17] Mas antes dessa época, em 1896, o bacteriologista Ernest Hanbury Hankin (1865–1939) relatou que algo nas águas do rio Ganges poderia matar Vibrio cholerae - a causa da cólera. O agente na água podia passar por filtros que removem as bactérias, mas era destruído pela fervura.[18]
Vírus de plantas[editar | editar código-fonte]
Em 1882, Adolf Mayer (1843–1942) descreveu uma condição das plantas de tabaco, que ele chamou de "doença do mosaico" ("mozaïkziekte"). As plantas doentes tinham folhas variegadas e pintadas.[19] Ele excluiu a possibilidade de uma infecção fúngica e não conseguiu detectar nenhuma bactéria e especulou que um "princípio infeccioso semelhante a uma enzima solúvel estava envolvido".[20] No entanto, ele não levou adiante sua ideia, de modo que os experimentos de filtração de Ivanovsky e Beijerinck sugeriram que a causa era um agente infeccioso anteriormente desconhecido. Depois que o mosaico do tabaco foi reconhecido como uma doença viral, foram descobertas infecções por vírus em muitas outras plantas.[20]
Século XX[editar | editar código-fonte]
No final do século XIX, os vírus eram definidos em termos de infectividade, capacidade de filtragem e necessidade de hospedeiros vivos. Até então, os vírus só haviam sido cultivados em plantas e animais, mas em 1906, Ross Granville Harrison (1870–1959) inventou um método para o crescimento de tecido na linfa,[21] e, em 1913, E. Steinhardt, C. Israeli, e R. A. Lambert usaram este método para cultivar o vírus vaccinia em fragmentos de tecido da córnea de porquinho da índia.[22] Em 1928, H. B. e M. C. Maitland cultivaram o vírus vaccinia em suspensões de rins de galinha picados.[23] Seu método não foi amplamente adotado até a década de 1950, quando o poliovírus foi cultivado em grande escala para a produção de vacinas.[24] Em 1941-1942, George Hirst (1909-1994) desenvolveu testes baseados na hemaglutinação para quantificar uma ampla gama de vírus, bem como anticorpos específicos para vírus no soro.[25][26]
Gripe[editar | editar código-fonte]

Embora o vírus da influenza que causou a pandemia de influenza de 1918-1919 não tenha sido descoberto até os anos 1930, as descrições da doença e pesquisas subsequentes provaram que ele foi o culpado.[27] A pandemia matou entre 40 e 50 milhões de pessoas em menos de um ano,[28] mas a prova de que foi causada por um vírus não foi obtida até 1933.[29] Haemophilus influenzae é uma bactéria oportunista que comumente segue infecções por influenza; isso levou o eminente bacteriologista alemão Richard Pfeiffer (1858–1945) a concluir incorretamente que essa bactéria era a causa da gripe.[30] Um grande avanço veio em 1931, quando o patologista norte-americano Ernest William Goodpasture desenvolveu influenza e vários outros vírus em ovos de galinha fertilizados.[31] Hirst identificou uma atividade enzimática associada à partícula do vírus, posteriormente caracterizada como neuraminidase, a primeira demonstração de que os vírus poderiam conter enzimas. Frank Macfarlane Burnet mostrou no início dos anos 1950 que o vírus se recombina em altas frequências, e Hirst mais tarde deduziu que ele tem um genoma segmentado.[32]
Final do século XX e início do século XXI[editar | editar código-fonte]

A segunda metade do século XX foi a idade de ouro da descoberta de vírus e a maioria das duas mil espécies reconhecidas de vírus animais, vegetais e bacterianos foram descobertas durante esses anos.[33][34] Em 1946, foi descoberta a diarreia por vírus bovino[35] que ainda é possivelmente o patógeno mais comum em bovinos em todo o mundo[36] e, em 1957, foi descoberto o arterivírus equino.[37] Na década de 1950, melhorias no isolamento de vírus e métodos de detecção resultaram na descoberta de vários vírus humanos importantes, incluindo o vírus varicela-zoster,[38] os paramixovírus,[39] - que incluem o vírus do sarampo[40] e o vírus sincicial respiratório[39] - e os rinovírus que causam o resfriado comum.[41] Na década de 1960, mais vírus foram descobertos. Em 1963, o vírus da hepatite B foi descoberto por Baruch Blumberg.[42] A transcriptase reversa, a enzima chave que os retrovírus usam para traduzir seu RNA em DNA, foi descrita pela primeira vez em 1970, independentemente por Howard Temin e David Baltimore.[43] Isso foi importante para o desenvolvimento de medicamentos antivirais - um momento decisivo na história das infecções virais.[44] Em 1983, Luc Montagnier (nascido em 1932) e sua equipe no Instituto Pasteur na França isolaram pela primeira vez o retrovírus agora chamado de HIV.[45] Em 1989, a equipe de Michael Houghton na Chiron Corporation descobriu a hepatite C.[46] Novos vírus e cepas de vírus foram descobertos em cada década da segunda metade do século XX. Essas descobertas continuaram no século XXI com o surgimento de novas doenças virais como a SARS[47] e o Nipah.[48] Apesar das conquistas dos cientistas nos últimos cem anos, os vírus continuam a representar novas ameaças e desafios.[49]
Avanços Recentes na Virologia e Seus Impactos Globais[editar | editar código-fonte]
A virologia tem desempenhado um papel fundamental na compreensão e no combate às doenças virais. No século XXI, esta área científica tem enfrentado o grande desafio do surgimento de novas doenças virais e tem registado progressos notáveis na prevenção e tratamento de infeções virais.
O desenvolvimento de vacinas modernas[editar | editar código-fonte]
As vacinas são a intervenção médica mais eficaz e económica disponível para combater doenças infecciosas. Estes consistem em preparação biológica que estimulam o sistema imunológico para fornecer imunidade protetora contra patógenos/agentes nocivos específicos. O design e o desenvolvimento de vacinas evoluíram ao longo dos anos. As primeiras vacinas foram criadas com pouca tecnologia e falta de conhecimentos básicos, representando pura façanha da engenhosidade humana. Em contraste, o desenvolvimento de vacinas modernas tira partido dos avanços tecnológicos e da nossa melhor compreensão do sistema imunitário e das interações entre agentes patogénicos e hospedeiros.[50] Devido à rápida disseminação global da pandemia da COVID-19, surgiu a urgência na busca do desenvolvimento de vacinas para conter a pandemia, levando a um esforço de pesquisadores de todo o mundo. A resposta à COVID-19 viu um notável desenvolvimento de vacinas que foi mais rápido do que qualquer outro visto anteriormente. As vacinas candidatas foram desenvolvidas e passaram por ensaios clínicos a partir da fase experimental, com os programas de desenvolvimento de vacinação concluídos em dezembro de 2020[51]. Ao contrário do habitual calendário de desenvolvimento de vacinas que varia entre 3 a 9 anos, foi evidente a notável rapidez com o qual foi criada a vacina contra a COVID-19, passando desde as primeiras publicações do sequenciamento do SARS-CoV-2 até à fase 1 em apenas 6 meses[52]. Ainda segundo [53], este ritmo acelerado se deu por diversos fatores: incluindo o conhecimento prévio do papel da proteína Spike (ou proteína S) na patogênese do coronavírus, provando que os anticorpos neutralizantes direcionados contra ao proteína S desempenham um papel fundamental na construção da imunidade. Sendo as abordagens mais aplicadas no desenvolvimento incluíram a utilização de ácidos nucléicos, vírus inativados ou vivos atenuados, vetores virais e proteínas recombinantes ou partículas de vírus[54]
Impactos na saúde pública e na medicina[editar | editar código-fonte]
Os avanços recentes na virologia tiveram um grande impacto na saúde pública e na medicina. O diagnóstico atempado de infecções virais, o desenvolvimento de tratamentos antivirais e vacinas eficazes contribuíram para a prevenção e tratamento de doenças virais, melhoria da qualidade de vida e redução da mortalidade. Sendo a vacinação o melhor método para prevenir e combater inúmeras doenças infecciosas e mortais [55]. Exemplificando sua eficácia, a erradicação da varíola e da poliomielite é notável[56][57]. Além do rápido desenvolvimento de vacina para controle da pandemia causada pelo vírus SARS-CoV-2.
Referências
- ↑ Bordenave G (maio de 2003). «Louis Pasteur (1822–1895)». Microbes and Infection / Institut Pasteur. 5: 553–60. PMID 12758285. doi:10.1016/S1286-4579(03)00075-3
- ↑ Shors 2008, pp. 76–77
- ↑ a b c Topley & Wilson 1998, p. 3
- ↑ Leppard, Keith; Nigel Dimmock; Easton, Andrew (2007). Introduction to Modern Virology. [S.l.]: Blackwell Publishing Limited. pp. 4–5. ISBN 978-1-4051-3645-7
- ↑ Fenner, F. (2009). «History of Virology: Vertebrate Viruses». In: Mahy; Van Regenmortal. Desk Encyclopedia of General Virology. Oxford, UK: Academic Press. ISBN 978-0-12-375146-1
- ↑ Staples JE, Monath TP (27 de agosto de 2008). «Yellow fever: 100 years of discovery». JAMA: The Journal of the American Medical Association. 300: 960–2. PMID 18728272. doi:10.1001/jama.300.8.960

- ↑ Chiong MA (dezembro de 1989). «Dr. Carlos Finlay and yellow fever». Canadian Medical Association Journal. 141: 1126. PMC 1451274
 . PMID 2684378
. PMID 2684378 - ↑ Litsios S (2001). «William Crawford Gorgas (1854–1920)». Perspectives in Biology and Medicine. 44: 368–78. PMC 1089739
 . PMID 11482006. doi:10.1353/pbm.2001.0051
. PMID 11482006. doi:10.1353/pbm.2001.0051 - ↑ Patterson R (setembro de 1989). «Dr. William Gorgas and his war with the mosquito». Canadian Medical Association Journal. 141: 596–7, 599. PMC 1451363
 . PMID 2673502
. PMID 2673502 - ↑ Frierson JG (junho de 2010). «The yellow fever vaccine: a history». Yale Journal of Biology and Medicine. 83: 77–85. PMC 2892770
 . PMID 20589188
. PMID 20589188 - ↑ From Ekspång, ed. (1993). Nobel Lectures, Physics 1981–1990. [S.l.]: World Scientific. ISBN 978-9810207281
- ↑ Carr, N. G.; Mahy, B. W. J.; Pattison, J. R.; Kelly, D. P. (1984). The Microbe 1984: Thirty-sixth Symposium of the Society for General Microbiology, held at the University of Warwick, April 1984. Col: Symposia of the Society for general microbiology. 36. [S.l.]: Cambridge University Press. ISBN 978-0-521-26056-5. OCLC 499302635
- ↑ Stanley WM, Loring HS (1936). «The isolation of crystalline tobacco mosaic virus protein from diseased tomato plants». Science. 83: 85. Bibcode:1936Sci....83...85S. PMID 17756690. doi:10.1126/science.83.2143.85
- ↑ Stanley WM, Lauffer MA (1939). «Disintegration of tobacco mosaic virus in urea solutions». Science. 89: 345–347. Bibcode:1939Sci....89..345S. PMID 17788438. doi:10.1126/science.89.2311.345
- ↑ Loring HS (1939). «Properties and hydrolytic products of nucleic acid from tobacco mosaic virus». Journal of Biological Chemistry. 130: 251–258
- ↑ Burton E. Tropp (2007). Molecular Biology: Genes to Proteins. Burton E. Tropp. Sudbury, Massachusetts: Jones & Bartlett Publishers. ISBN 978-0-7637-5963-6
- ↑ Shors, Teri (2008). Understanding Viruses. Sudbury, Mass: Jones & Bartlett Publishers. ISBN 978-0-7637-2932-5
- ↑ Ackermann, H-W (2009). «History of Virology: Bacteriophages». Desk Encyclopedia of General Virology. [S.l.: s.n.]
- ↑ Mayer A (1882) Over de moza¨ıkziekte van de tabak: voorloopige mededeeling. Tijdschr Landbouwkunde Groningen 2: 359–364 (In German)
- ↑ a b Quoted in: van der Want JP, Dijkstra J (agosto de 2006). «A history of plant virology». Archives of Virology. 151: 1467–98. PMID 16732421. doi:10.1007/s00705-006-0782-3
- ↑ Nicholas, J.S. (1961). Ross Granville Harrison 1870—1959 A Biographical Memoir (PDF). [S.l.]: National Academy of Sciences
- ↑ Steinhardt, E.; Israeli, C.; Lambert, R.A. (1913). «Studies on the cultivation of the virus of vaccinia» (PDF). J. Inf Dis. 13: 294–300. doi:10.1093/infdis/13.2.294
- ↑ Maitland HB, Magrath DI (setembro de 1957). «The growth in vitro of vaccinia virus in chick embryo chorio-allantoic membrane, minced embryo and cell suspensions». The Journal of Hygiene. 55: 347–60. PMC 2217967
 . PMID 13475780. doi:10.1017/S0022172400037268
. PMID 13475780. doi:10.1017/S0022172400037268 - ↑ Sussman, Max; Topley, W.W.C.; Wilson, Graham K.; Collier, L.H.; Balows, Albert (1998). Topley & Wilson's microbiology and microbial infections. London: Arnold. ISBN 978-0-340-66316-5
- ↑ Joklik WK (maio de 1999). «When two is better than one: thoughts on three decades of interaction between Virology and the Journal of Virology». J. Virol. 73: 3520–3. PMC 104123
 . PMID 10196240
. PMID 10196240 - ↑ Schlesinger RW, Granoff A (1994). «George K. Hirst (1909–1994)». Virology. 200: 327. doi:10.1006/viro.1994.1196
- ↑ Shors 2008, pp. 238–344
- ↑ Oldstone, Michael B. A. (2009). Viruses, Plagues, and History: Past, Present and Future. [S.l.]: Oxford University Press. ISBN 978-0-19-532731-1
- ↑ Cunha BA (março de 2004). «Influenza: historical aspects of epidemics and pandemics». Infectious Disease Clinics of North America. 18: 141–55. PMID 15081510. doi:10.1016/S0891-5520(03)00095-3
- ↑ Oldstone 2009, p. 315
- ↑ Goodpasture EW, Woodruff AM, Buddingh GJ (1931). «The cultivation of vaccine and other viruses in the chorioallantoic membrane of chick embryos». Science. 74: 371–2. Bibcode:1931Sci....74..371G. PMID 17810781. doi:10.1126/science.74.1919.371
- ↑ Kilbourne ED (novembro de 1975). «Presentation of the Academy Medal to George K. Hirst, M.D». Bull N Y Acad Med. 51: 1133–6. PMC 1749565
 . PMID 1104014
. PMID 1104014 - ↑ Norrby E (2008). «Nobel Prizes and the emerging virus concept». Archives of Virology. 153: 1109–23. PMID 18446425. doi:10.1007/s00705-008-0088-8
- ↑ «Discoverers and Discoveries - ICTV Files and Discussions». 11 de novembro de 2009. Consultado em 5 de novembro de 2017. Cópia arquivada em 11 de novembro de 2009
- ↑ Olafson P, MacCallum AD, Fox FH (julho de 1946). «An apparently new transmissible disease of cattle». The Cornell Veterinarian. 36: 205–13. PMID 20995890
- ↑ Peterhans E, Bachofen C, Stalder H, Schweizer M (2010). «Cytopathic bovine viral diarrhea viruses (BVDV): emerging pestiviruses doomed to extinction». Veterinary Research. 41: 44. PMC 2850149
 . PMID 20197026. doi:10.1051/vetres/2010016
. PMID 20197026. doi:10.1051/vetres/2010016 - ↑ Bryans JT, Crowe ME, Doll ER, McCollum WH (janeiro de 1957). «Isolation of a filterable agent causing arteritis of horses and abortion by mares; its differentiation from the equine abortion (influenza) virus». The Cornell Veterinarian. 47: 3–41. PMID 13397177
- ↑ Weller TH (dezembro de 1995). «Varicella-zoster virus: History, perspectives, and evolving concerns». Neurology. 45: S9–10. PMID 8545033. doi:10.1212/wnl.45.12_suppl_8.s9
- ↑ a b Schmidt AC, Johnson TR, Openshaw PJ, Braciale TJ, Falsey AR, Anderson LJ, Wertz GW, Groothuis JR, Prince GA, Melero JA, Graham BS (novembro de 2004). «Respiratory syncytial virus and other pneumoviruses: a review of the international symposium—RSV 2003». Virus Research. 106: 1–13. PMID 15522442. doi:10.1016/j.virusres.2004.06.008
- ↑ Measles: old vaccines, new vaccines. Col: Current Topics in Microbiology and Immunology. 330. [S.l.: s.n.] 2009. pp. 191–212. ISBN 978-3-540-70616-8. PMID 19203111. doi:10.1007/978-3-540-70617-5_10
- ↑ Tyrrell DA (agosto de 1987). «The common cold—my favourite infection. The eighteenth Majority Stephenson memorial lecture». The Journal of General Virology. 68: 2053–61. PMID 3039038. doi:10.1099/0022-1317-68-8-2053

- ↑ Zetterström R (março de 2008). «Nobel Prize to Baruch Blumberg for the discovery of the aetiology of hepatitis B». Acta Paediatrica. 97: 384–7. PMID 18298788. doi:10.1111/j.1651-2227.2008.00669.x
- ↑ RNA-directed DNA synthesis and RNA tumor viruses. Col: Advances in Virus Research. 17. [S.l.: s.n.] 1972. pp. 129–86. ISBN 9780120398171. PMID 4348509. doi:10.1016/S0065-3527(08)60749-6
- ↑ Broder S (janeiro de 2010). «The development of antiretroviral therapy and its impact on the HIV-1/AIDS pandemic». Antiviral Research. 85: 1–18. PMC 2815149
 . PMID 20018391. doi:10.1016/j.antiviral.2009.10.002
. PMID 20018391. doi:10.1016/j.antiviral.2009.10.002 - ↑ Barré-Sinoussi F, Chermann JC, Rey F, Nugeyre MT, Chamaret S, Gruest J, Dauguet C, Axler-Blin C, Vézinet-Brun F, Rouzioux C, Rozenbaum W, Montagnier L (maio de 1983). «Isolation of a T-lymphotropic retrovirus from a patient at risk for acquired immune deficiency syndrome (AIDS)». Science. 220: 868–71. Bibcode:1983Sci...220..868B. PMID 6189183. doi:10.1126/science.6189183
- ↑ Houghton M (novembro de 2009). «The long and winding road leading to the identification of the hepatitis C virus». Journal of Hepatology. 51: 939–48. PMID 19781804. doi:10.1016/j.jhep.2009.08.004

- ↑ Detection of SARS Coronavirus. Col: Methods in Molecular Biology. 665. [S.l.: s.n.] 2011. pp. 369–82. ISBN 978-1-60761-816-4. PMID 21116811. doi:10.1007/978-1-60761-817-1_20
- ↑ Field H, Young P, Yob JM, Mills J, Hall L, Mackenzie J (abril de 2001). «The natural history of Hendra and Nipah viruses». Microbes and Infection / Institut Pasteur. 3: 307–14. PMID 11334748. doi:10.1016/S1286-4579(01)01384-3
- ↑ Mahy, B.W.J. (2009). Desk Encyclopedia of Human and Medical Virology. Boston: Academic Press. pp. 583–7. ISBN 978-0-12-375147-8
- ↑ Fiyouzi, Tara; Reche, Pedro A. (2023). Reche, Pedro A., ed. «Vaccine Design: An Introduction». New York, NY: Springer US (em inglês): 1–14. ISBN 978-1-0716-3238-3. doi:10.1007/978-1-0716-3239-0_1. Consultado em 20 de setembro de 2023
- ↑ Ball, Philip (18 de dezembro de 2020). «The lightning-fast quest for COVID vaccines — and what it means for other diseases». Nature (7840): 16–18. ISSN 0028-0836. doi:10.1038/d41586-020-03626-1. Consultado em 20 de setembro de 2023
- ↑ Heaton, Penny M. (12 de novembro de 2020). «The Covid-19 Vaccine-Development Multiverse». New England Journal of Medicine (em inglês) (20): 1986–1988. ISSN 0028-4793. PMC PMC7377255
 Verifique
Verifique |pmc=(ajuda). PMID 32663910. doi:10.1056/NEJMe2025111. Consultado em 20 de setembro de 2023 - ↑ Heaton, Penny M. (12 de novembro de 2020). «The Covid-19 Vaccine-Development Multiverse». New England Journal of Medicine (em inglês) (20): 1986–1988. ISSN 0028-4793. PMC PMC7377255
 Verifique
Verifique |pmc=(ajuda). PMID 32663910. doi:10.1056/NEJMe2025111. Consultado em 20 de setembro de 2023 - ↑ Wiersinga, W. Joost; Rhodes, Andrew; Cheng, Allen C.; Peacock, Sharon J.; Prescott, Hallie C. (25 de agosto de 2020). «Pathophysiology, Transmission, Diagnosis, and Treatment of Coronavirus Disease 2019 (COVID-19)». JAMA (8). 782 páginas. ISSN 0098-7484. doi:10.1001/jama.2020.12839. Consultado em 20 de setembro de 2023
- ↑ Chakraborty, Chiranjib; Bhattacharya, Manojit; Dhama, Kuldeep (17 de março de 2023). «SARS-CoV-2 Vaccines, Vaccine Development Technologies, and Significant Efforts in Vaccine Development during the Pandemic: The Lessons Learned Might Help to Fight against the Next Pandemic». Vaccines (em inglês) (3). 682 páginas. ISSN 2076-393X. PMC PMC10054865
 Verifique
Verifique |pmc=(ajuda). PMID 36992266 Verifique|pmid=(ajuda). doi:10.3390/vaccines11030682. Consultado em 20 de setembro de 2023 - ↑ Okwo-Bele, Jean-Marie; Cherian, Thomas (30 de dezembro de 2011). «The expanded programme on immunization: A lasting legacy of smallpox eradication». Vaccine. Smallpox Eradication after 30 Years: Lessons, Legacies and Innovations: D74–D79. ISSN 0264-410X. doi:10.1016/j.vaccine.2012.01.080. Consultado em 20 de setembro de 2023
- ↑ Javed, Haseeba; Rizvi, Musa Ali; Fahim, Zara; Ehsan, Muhammad; Javed, Mubeena; Raza, Muhammad Asad (25 de novembro de 2022). «Global polio eradication; can we replicate the smallpox success story?». Reviews in Medical Virology (3). ISSN 1052-9276. doi:10.1002/rmv.2409. Consultado em 20 de setembro de 2023
