Abrine

| Abrine (Abrus precatorius) | ||||
|---|---|---|---|---|
 | ||||
| Identificatie | ||||
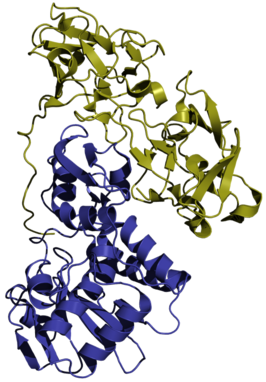
| PDB-codes | 1ABR | |||
| Externe identificaties | ||||
| UniProt | P11140 | |||
| ||||
Abrine is een fytotoxine afkomstig van het paternosterboontje van de plant Abrus precatorius uit het abrusgeslacht. De naam abrine leidt vaak tot verwarring met de Engelse term “abrine” wat voor N-methyl-L-tryptofaan[1] staat. De correcte Engelse naam is abrin.
Abrus precatorius komt voornamelijk in tropische en subtropische streken in Zuidoost-Azië voor. De bonen werden voornamelijk als sieraden gebruikt wegens hun dieprode kleur met een zwarte stip. Hoewel de bonen vaak als halsketting worden gebruikt zijn tot nu toe weinig overlijdensgevallen vermeld.[2] Dit heeft vooral met de harde schaal van de bonen te maken die bij consumptie niet kan worden verteerd. Desondanks mag de toxiciteit van abrine niet worden onderschat. Abrine geldt als een van de giftigste stoffen op aarde die qua werking sterk met ricine overeenkomt.
Symptomen[bewerken | brontekst bewerken]
Abrine en ricine zijn allebei fytotoxinen met dezelfde toxische mechanismen. Het enige, maar belangrijkste verschil in toxiciteit is dat abrine in muizen 75 keer toxischer is dan ricine (0.04µg/kg voor abrine in tegenstelling tot 3µg/kg voor ricine). Verder zijn de symptomen van deze twee fytotoxinen gelijk.
Afhankelijk van de verkregen dosis en de blootstellingroute komt het na ca 36-72 uren na de blootstelling tot overlijden. De belangrijkste blootstellingsroutes zijn via inhalatie, digestie en absorptie.
Inhalatie[bewerken | brontekst bewerken]
Als abrine wordt ingeademd als aerosol komt het binnen acht uur tot verschillende symptomen. Daaronder verzwaard ademen (respiratory distress), koorts, hoest, benauwdheid, misselijkheid. Dit wordt gevolgd door hevig transpireren, de ontwikkeling van een longoedeem, cyanose, hypotensie en leidt uiteindelijk tot het uitblijven van de ademhaling en tot lage bloeddruk. De vloeistof in de long kan worden gediagnosticeerd door een röntgenfoto of door afluisteren met een stethoscoop.
Digestie[bewerken | brontekst bewerken]
Een orale opname van abrine kan leiden tot misselijkheid en diarree met gastro-intestinale versterkte bloedingsneiging. Dehydratie, gevolgd door hypotensie en bloed in de urine is het resultaat. Dit leidt uiteindelijk tot necrose van lever, milt en nier en de mens kan daaraan overlijden.
Absorptie[bewerken | brontekst bewerken]
Blootstelling van de huid en van de ogen zorgt voor irritatie, roodheid en pijn. Als er wonden zijn kan abrine ook via de huid worden opgenomen, maar opname door intacte huid is niet te verwachten, zolang het gif niet is opgelost in een stof die de absorptie bevordert.
Andere toxische effecten[bewerken | brontekst bewerken]
Een intramusculaire intoxicatie zorgt voor lokale pijn, spier- en Lymfekliernecrose. Verder belangrijk is leukocytose die constant bij mensen optreedt door vergiftiging via de long of de darm. Het aantal witte bloedcellen stijgt met een factor 2-5 boven de fysiologische waarden[3].[4]
Biochemie en structuur[bewerken | brontekst bewerken]
De toxische werking van abrine berust op het vermogen van de stof om cellen binnen te dringen en hier de eiwitsynthese tot stilstand te brengen. Deze acties zijn sterk gerelateerd aan de moleculaire structuur van abrine. Door middel van een interactie met een koolhydraatketen op de celoppervlak kan abrine zich vasthechten en wordt vervolgens de cel in getransporteerd. In het binnenste van de cel verstoort abrine een van de ribosomale subunits en vermindert dus de eiwitsynthese van de cel. Twee structuren, namelijk de alfa- en bètaketen, van abrine zijn hierbij betrokken. Abrine wordt gesynthetiseerd als een polypeptidenketen, die later in twee functionele ketens gesplitst wordt. De resulterende bètaketen bindt aan uitwendige celmembraanreceptoren, wat nodig is voor de opname van abrine. De alfaketen is enzymatisch aan het ribosoom actief. Op basis van de structuur van de actieve delen van abrine is het potentieel mogelijk om het te remmen en zo de toxiciteit te bestrijden.[5] De structuur van abrine komt sterk overeen met de structuur van het gift ricine.
Alfaketen[bewerken | brontekst bewerken]
De toxisch-moleculaire werking van abrine berust op de enzymatische werking van de alfaketen. Deze splitst adenine aan positie A4324 door hydrolyse van de N-glycosidische binding van de 28S-rRNA subunit, die onderdeel is van de 60S subunit van een ribosoom. Het toxine verbreekt de RNA-keten alleen indirect, omdat de net door de alfaketen gedepurineerde RNA meer vatbaar is voor hydrolyse in aanwezigheid van een basische pH dan onaangetaste RNA. Als aniline aanwezig is kan depurinatie ook onder een zure pH plaatsvinden. De alfaketens zijn zeer efficiënt en één molecuul is in staat om per minuut meerdere duizend ribosomen te inactiveren. Eén abrine molecuul is al voldoende om meer ribosomen te inactiveren dan de cel binnen dezelfde tijd kan aanmaken. Dit resulteert in celletaliteit. Alfaketens bevatten bovendien weinig lysine wat een potentiële bescherming tegen afbraak door proteasomen is, omdat het eiwitmarkerende polyubiquitine niet kan binden.[6]
Cellen bevatten ook vanuit de natuur eiwitten met abrine-typische eigenschappen, namelijk ribosome inactivating protein (RIP II), echter zijn deze non-toxisch omdat de bètaketen ontbreekt waardoor ze zich niet aan cellen kunnen hechten om deze binnen te dringen.[7]
Bètaketen[bewerken | brontekst bewerken]
De meeste celmembranen bevatten naast hun fosfolipidebilayer ook uitwendige koolhydraat (suiker)-gerelateerde groepen, namelijk glycoproteïnen en glycolipiden. Alleen de bètaketen bezit, zoals lectine, de capaciteit om suikers, voornamelijk galactose, te binden. Dit vermogen levert abrine de mogelijkheid op om aan cellen uitwendig te hechten. Opname blijkt mogelijk te zijn via caveolae-gerelateerde endocytose. Andere opname mogelijkheden zijn niet goed onderzocht.
Absorptie Distributie Metabolisme Excretie Toxiciteit (ADMET)[bewerken | brontekst bewerken]
De route van absorptie bepaalt voor een deel de symptomen. Komt de stof na absorptie in de bloedbaan terecht beïnvloedt het de lever en nieren (zie symptomen). De toxiciteit is maximaal bij een neutrale of licht alkalische pH. Abrine wordt opgenomen in de cellen via endocytose.[8] De alfa-keten van abrine interageert met de glycoproteïnen in de gal bèta-1- en gal alpha-1-antilichamen, maar het reageert maar zwak met de glycoproteïnen op de bloedcellen. Het kan ook monosacharide met een bepaalde configuratie binden.[9]
Er is echter geen activatie van abrine door het metabolisme nodig. Alleen de directe chemische eigenschappen van het eiwit zijn verantwoordelijk voor zijn toxiciteit.
Blootstelling aan abrine leidt uiteindelijk tot een inhibitie van de proteïnsynthese, waardoor celdood optreedt. Ook caspase 3 wordt geactiveerd door abrine. Dit leidt tot apoptose. Daardoor wordt onder andere schade in het endotheel veroorzaakt, zodat de capillairen sterker permeabel worden en vloeistoffen en proteïnen lekken. Er treden dus weefseloedeem op (vascular-leak-syndrome).[10] Excretie vindt plaats via de urine. Abrine blijft echter tot 40-50 uur in het lichaam en wordt daarmee veel langzamer uitgescheiden dan ricine. In combinatie met lactose accumuleert het eiwit in de lever[11] en verhoogt dus de toxiciteit in sterke mate.
Kankerbestrijding[bewerken | brontekst bewerken]
Sinds jaren wordt geprobeerd de manier waarop abrine de cel binnen komt te gebruiken om kanker te bestrijden. Vooral de bètaketen staat in de focus omdat koppeling met cellulaire suikergroepen kankercellen buiten werk kan stellen. Maar ook abrine zelf wordt gebruikt om tumoren te bevechten. Recente studies laten zien dat de overlevingskans bij dieren met kanker groter was bij behandeling met ABP (abrin-derived peptide) wat apoptose van de kankercellen induceert.[12]
Nobelprijs[bewerken | brontekst bewerken]
In 1908 won Paul Ehrlich de Nobelprijs voor de Fysiologie of Geneeskunde samen met Ilja Iljitsj Metsjnikov.[13] Ehrlich ging 1891 de mythe na dat kalveren in India resistenties tegen abrine kunnen opbouwen als deze met een lage dosis van het gif worden gevoerd. Bij de analyse van dierserum vond Ehrlich proteïnen die de toxine konden binden en neerslaan. Later bleek dat deze proteïnen antilichamen waren die verantwoordelijk waren voor de neerslag. Voor ricine bleven de dieren echter nog gevoelig waardoor Ehrlich concludeerde dat een antilichaam tegen een specifiek antigeen wordt gemaakt.
Zie ook[bewerken | brontekst bewerken]
Bronnen, noten en/of referenties
|