リン酸銀

| リン酸銀 | |
|---|---|
 | |
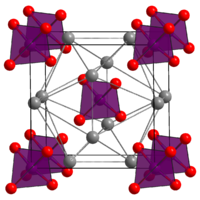 | |
Silver(I) phosphate | |
別称 オルトリン酸銀、リン酸銀(I) | |
| 識別情報 | |
| CAS登録番号 | 7784-09-0 |
| ChemSpider | 140592 |
| EC番号 | 232-049-0 |
| 特性[1] | |
| 化学式 | Ag3O4P |
| モル質量 | 418.58 g mol−1 |
| 外観 | 黄色の粉末で、感光により暗色化 |
| 匂い | 無臭 |
| 密度 | 6.37 g/cm3 |
| 融点 | 849 °C |
| 沸点 | (分解) |
| 水への溶解度 | 0.65mg/100ml(20℃) |
| 溶解度 | 希硝酸、アンモニア水、炭酸アンモニウム溶液に可溶。希酢酸などの弱酸溶液には微溶。 |
| 危険性 | |
| 引火点 | (不燃性) |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
リン酸銀(リンさんぎん、英: Silver phosphate)は、化学式Ag3PO4で表される、銀のリン酸塩。オルトリン酸銀、リン酸銀(I) とも呼ばれる。黄色の粉末で、光反応性がある。
性質[編集]
硝酸銀とオルトリン酸液の反応により、黄色の沈殿物として生じる[2]。溶解度積は8.89×10-17 mol4dm-12である[3][4]。この沈殿反応は分析的に重要であり[5]、リン酸塩の定性的・定量的試験に使用できる。
硝酸やアンモニアに可溶であり[2]、リン酸銀のアンモニア溶液から徐々にアンモニアを除去することにより、リン酸銀の大きな結晶を得られる。この反応は、リン酸イオンの定量分析に使用できる[6]。異なる結晶状態のリン酸銀に対し、同じ格子構造を造り出せる[6]。
用途[編集]
主な用途として分析化学や、細胞組織等の銀染色に用いられる[7]。抗菌目的で素材に銀イオンを組み込むことへの利用も考えられている[8]。また、感光剤として初期の写真材料に使用された[9]。
光触媒の1つとして、強い光酸化性を持つ。メチレンブルーを使った光酸化分解実験では、比較対象の酸化チタンやバナジン酸ビスマスの数十倍、90%近い量子収率の光酸化性能を示した。可視光線下での水の光酸化分解においても、バナジン酸ビスマスや酸化タングステン(VI)をしのぐ性能を示しており、人工光合成への応用が期待されている[10]。
安全性[編集]
日本の毒物及び劇物取締法では、無機銀塩類の1つとして劇物に指定されている。飲み込むと嘔吐、腹痛、下痢の症状が現れることがある。不燃性であるが、加熱により酸化銀(I)およびリンの酸化物に分解する[1]。
その他の銀のリン酸塩[編集]
- ピロリン酸銀 Ag4P2O7 (CAS No. 13465-97-9)[11]
- 銀と二リン酸の反応により得られる、白色の沈殿。オルトリン酸銀同様に光に敏感であり、光の曝露で赤色に変色する[12]。密度は5.306g/cm3、融点は585℃である[13]。水和物は110℃で分解する[13]。
- メタリン酸銀 (AgPO3) (CAS No. 13465-96-8)[14]
- 白色の固体で、密度は6.370g/cm3、融点は482℃である。水和物は240℃で分解する[13]。
脚注[編集]
- ^ a b 化学物質等安全データシート (PDF) (昭和化学)
- ^ a b Phosphates Archived 2010年8月28日, at the Wayback Machine. www.1911encyclopedia.org
- ^ Ksp solubility constant for common salts www.solubilityofthing.com
- ^ SOLUBILITY PRODUCT CONSTANTS Archived 2012年6月15日, at the Wayback Machine. www.ktf-split.hr
- ^ Inorganic chemistry , Egon Wiberg, Nils Wiberg, Arnold Frederick Holleman , Academic Press , 2001] p.721 Google Books excerpt
- ^ a b F.H. Firsching (1961). “Precipitation of Silver Phosphate from Homogenous Solution”. Anal. Chem. 33 (7): 873. doi:10.1021/ac60175a018.
- ^ Taichman, Russell S.; Hauschka, Peter V. (1992). “Effects of interleukin-1? and tumor necrosis factor-? on osteoblastic expression of osteocalcin and mineralized extracellular matrix in vitro”. Inflammation 16 (6): 587–601. doi:10.1007/BF00919342. ISSN 0360-3997. Free version
- ^ Nanocoated film as a bacteria killer 23/1/2009 , www.nanowerk.com
- ^ Cassell's cyclopaedia of photography , Bernard Edward Jones , Ayer Publishing , 1973 , p.401 'Phosphate plates and papers' , googlebooks link
- ^ “高活性光触媒リン酸銀の発見と環境再生の期待” (PDF). 独立行政法人物質・材料研究機構. 2016年1月14日閲覧。
- ^ Silver pyrophosphate www.chemicalbook.com
- ^ Silver Compounds p.5 , section 2.22 , from Kirk-Othmer Encyclopedia of Chemical Technology , Authors: SAMUEL F. ETRIS (The Silver Institute), C. ROBERT CAPPEL (Eastman Kodak Company) , via www.scribd.com
- ^ a b c Bulletin of the National Research Council , National Research Council (U.S.A) , 1950 , pp.56-57 google books link
- ^ Silver metaphosphate www.chemicalbook.com