Ibritumomab tiuxetan

| Ibritumomab tiuxetan | |
|---|---|
 | |
| Caratteristiche generali | |
| Massa molecolare (u) | g·mol-1 |
| Numero CAS | |
| Codice ATC | V10 |
| DrugBank | DB00078 |
| Proprietà chimico-fisiche | |
| Temperatura di fusione | ° C |
| Temperatura di ebollizione | ° C |
| Dati farmacologici | |
| Modalità di somministrazione | Endovena |
| Indicazioni di sicurezza | |
L'ibritumomab tiuxetano, in commercio con il nome di Zevalin, è un anticorpo monoclonale per il trattamento radioimmunoterapico di alcune forme di cellule B di linfoma non Hodgkin, che è un disordine linfoproliferativo del sistema linfatico. Il farmaco utilizza l'anticorpo IgG1 monoclonale di topo: ibritumomab in collaborazione con il chelante tiuxetano, a cui viene aggiunto un isotopo radioattivo a base di ittrio-90 o indio-111.
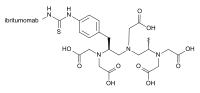
L'ibritumomab è una versione modificata del DTPA carbonio (Acido pentenico o Acido Dietilene triamine pentaacetico (DTPA)) nella cui struttura chimica è contenuto un gruppo isotiocianatobenzilico e un gruppo metilico.[1][2]
Storia[modifica | modifica wikitesto]
Sviluppato dalla IDEC Pharmaceuticals, ora diventata Biogen Idec, l'anticorpo tiuxetano è stato il primo farmaco radioimmunoterapico approvato dalla Food and Drug Administration (FDA) nel 2002 per il trattamento dei tumori. È stato approvato per il trattamento di pazienti con linfoma non Hodgkin (NHL) in recidiva, inclusi i pazienti con LNH follicolare refrattario al rituximab.
Nel dicembre 2007, la Cell Therapeutics Inc ha acquisito per gli USA i diritti di vendita, commercializzazione e distribuzione di questo anticorpo radioimmunoterapico dalla Biogen per circa 30 milioni di dollari. Al di fuori degli Stati Uniti, è la Bayer Schering Pharma che possiede i diritti di commercializzazione del farmaco.
Nel marzo 2009, Spectrum Pharmaceuticals ha acquisito i diritti per commercializzare lo Zevalin negli Stati Uniti; ed ora la Spectrum Pharmaceuticals è responsabile di tutte le attività relative a Zevalin negli Stati Uniti.
Nel settembre 2009, l'anticorpo tiuxetano ha ottenuto l'approvazione dalla FDA per l'indicazione più importante: trattamento dei pazienti con linfoma follicolare non-Hodgkin (NHL) non precedentemente trattati, che raggiungono una risposta parziale o completa alla chemioterapia di prima linea.
Ibritumomab è sotto copertura brevettuale, ed è attualmente il farmaco più costoso per singola dose disponibile negli USA (24000 $). Va però precisato che la terapia con il farmaco ha un equivalente farmacoeconomico vantaggioso per la riduzione dei tempi di trattamento.
Farmacologia[modifica | modifica wikitesto]
L'anticorpo si lega all'antigene CD20 che si trova sulla superficie delle cellule B sane e tumorali ma non sui precursori di queste. L'isotopo radioattivo legato all'anticorpo uccide le cellule cui si lega e quelle circostanti. Inoltre, lo stesso anticorpo può innescare la morte cellulare cellulo-mediata citotossicca anticorpo-dipendente (ADCC), la citotossicità complemento-dipendente (CDC), e l'apoptosi. Tutte insieme queste azioni eliminano le cellule B dall'organismo affetto da linfoma non Hodgkin permettendo ad una nuova popolazione di cellule sane B di svilupparsi partendo dalle cellule staminali linfoidi.
Note[modifica | modifica wikitesto]
- ^ Diane E. Milenic, Brady, Erik D.; Brechbiel, Martin W., Antibody-targeted radiation cancer therapy, in Nat Rev Drug Discov, vol. 3, n. 6, 2004-06, pp. 488–499, DOI:10.1038/nrd1413, ISSN 1474-1776, PMID 15173838. URL consultato il 17 aprile 2009.
- ^ WHO Drug Information
Bibliografia[modifica | modifica wikitesto]
- Frank Ashall, Le grandi scoperte scientifiche, Armando Editore, 1999, pp. 245–, ISBN 978-88-7144-949-4.
- Abul K. Abbas, Andrew H. Lichtman e Shiv Pillai, Immunologia cellulare e molecolare, Elsevier srl, 2010, pp. 79–, ISBN 978-88-214-3176-0.
- accessdate Abul K. Abbas e Andrew H. Lichtman, Le basi dell'immunologia, Elsevier srl, 2006, pp. 70–, ISBN 978-88-85675-85-8.
- accessdate Humphrey P. Rang, M. Maureen Dale e James M. Ritter, Farmacologia, Elsevier srl, 2008, pp. 778–, ISBN 978-88-214-3023-7.
- Enzo Fagiolo, Immunoematologia, Mediserve s.r.l., 2007, pp. 16–, ISBN 978-88-8204-135-9.
- Paolo Larizza, Trattato di medicina interna, PICCIN, 2005, pp. 909–, ISBN 978-88-299-1721-1.
- Angelo Sghirlanzoni, Terapia Delle Malattie Neurologiche, Springer, 3 aprile 2010, pp. 113–, ISBN 978-88-470-1119-9.
- Thomas C. King, Patologia, Elsevier srl, 2008, pp. 156–, ISBN 978-88-214-3019-0.
- (EN) whqlibdoc.who.int (archiviato dall'url originale il 16 ottobre 2009).
- (EN) Marie A. Simmons, Monoclonal antibodies: new research, Nova Publishers, 2005, ISBN 978-1-59454-247-3.
- (EN) Zhiqiang An, Therapeutic Monoclonal Antibodies: From Bench to Clinic, John Wiley and Sons, 8 settembre 2009, ISBN 978-0-470-11791-0.
- (EN) James W. Goding, Monoclonal antibodies: principles and practice : production and application of monoclonal antibodies in cell biology, biochemistry and immunology, Academic Press, 1996, ISBN 978-0-12-287023-1.
- (EN) Steve Shire, Current Trends in Monoclonal Antibody Development and Manufacturing, Springer, aprile 2009, ISBN 978-0-387-76642-3.
Ibritumomab tiuxetan[modifica | modifica wikitesto]
- (EN) Gopal B. Saha, Fundamentals of Nuclear Pharmacy, Springer, 14 novembre 2010, pp. 328–, ISBN 978-1-4419-5859-4.
- (EN) Connie Henke Yarbro, Debra Wujcik e Barbara Holmes Gobel, Cancer Nursing: Principles and Practice, Jones & Bartlett Learning, 21 aprile 2010, pp. 794–, ISBN 978-0-7637-6357-2.
- (EN) Gail M. Wilkes, Gail M Wilkes, R.N., M.S., Margaret Barton-Burke, Margaret Barton-Burke, R.N., PH.D., Oncology Nursing Drug Handbook 2011, Jones & Bartlett Publishers, 14 dicembre 2010, pp. 575–, ISBN 978-1-4496-0013-6.
- (EN) Tod W. Speer, Targeted Radionuclide Therapy, Lippincott Williams & Wilkins, 15 novembre 2010, pp. 1–, ISBN 978-0-7817-9693-4.
- (EN) Michael R. Bishop, Hematopoietic Stem Cell Transplantation, Springer, 2009, pp. 305–, ISBN 978-0-387-78579-0.
Collegamenti esterni[modifica | modifica wikitesto]
- www.zevalin.com, su zevalin.com.
- www.spectrumpharm.com, su spectrumpharm.com.