Microchimérisme

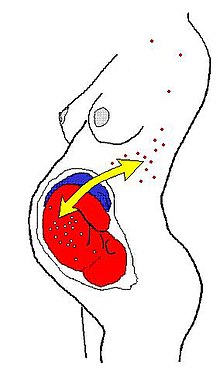
Le microchimérisme désigne la présence chez un individu d'un petit nombre de cellules issues d'un autre individu et donc génétiquement distinctes.
Il peut être lié à certains types de maladies auto-immunes bien que les mécanismes responsables ne soient pas clairs.
Sémantique et étymologie[modifier | modifier le code]
Le terme vient du préfixe « micro » et du mot « chimérisme » basé sur la Chimère hybride de la mythologie grecque. Le microchimérisme a été conceptualisé dans les années 60 et s’est répandu dans les années 70[1].
Typologie[modifier | modifier le code]
Chez l'Humain[modifier | modifier le code]
Chez l'humain (et peut-être chez tous les placentaires), la forme la plus courante est le microchimérisme fœto-maternel (également connu sous le nom de microchimérisme cellulaire fœtal ou chimérisme fœtal) dans lequel les cellules d'un fœtus traversent le placenta et établissent des lignées cellulaires au sein de la mère. Certaines de ces cellules fœtales peuvent persister et se multiplier chez la mère durant des décennies[2],[3].
Le phénotype exact de ces cellules est inconnu, mais plusieurs types de cellules ont déjà été identifiés, dont diverses lignées immunitaires, des cellules souches mésenchymateuses et des cellules dérivées du placenta[4]. Une étude réalisée en 2012 au Fred Hutchinson Cancer Research Center, à Seattle, a détecté des cellules avec le chromosome Y dans plusieurs zones du cerveau de femmes décédées[5].
Le microchimérisme fœto-maternel survient lors de la grossesse et peu de temps après l'accouchement chez la plupart des femmes (toutes n'hébergent pas de cellules fœtales après la grossesse)[réf. souhaitée]. Des études suggèrent que le microchimérisme fœto-maternel pourrait être influencé par les ligands de type immunoglobine des cellules tueuses (KIR)[6]. Les lymphocytes influencent aussi le développement d'un microchimérisme fœto-maternel persistant puisque les cellules tueuses naturelles composent environ 70 % des lymphocytes au cours du premier trimestre de la grossesse. Les motifs KIR sur les cellules tueuses naturelles maternelles de la mère et les ligands KIR sur les cellules fœtales pourraient avoir un effet sur le microchimérisme fœto-maternel. Dans une étude, les mères atteintes de KIR2DS1 présentaient des niveaux plus élevés de microchimérisme fœto-maternel par rapport aux mères qui étaient négatives pour ce KIR activateur[6].
Conséquences potentielles de ces cellules sur la santé ?[modifier | modifier le code]
Elles sont inconnues. Une hypothèse est que ces cellules fœtales pourraient déclencher une réaction du greffon contre l'hôte conduisant à une maladie auto-immune. Ceci expliquerait pourquoi de nombreuses maladies auto-immunes sont plus répandues chez les femmes d'âge moyen[7].
Une autre hypothèse est que les cellules fœtales rejoignent des tissus maternels blessés ou malades où elles agissent comme des cellules souches et participent à la réparation[8],[9].
Ces cellules fœtales pourraient aussi n'être que des passants innocents sans aucun effet sur la santé maternelle[10].
Après l'accouchement, 50 à 75 % des femmes hébergent des lignées cellulaires immunitaires fœtales. Des cellules immunitaires maternelles se retrouvent aussi dans le fœtus produisant un microchimérisme maternel → fœtal, mais ce phénomène serait environ deux fois moins fréquent que le premier[11].
Le microchimérisme fœto-maternel est particulièrement répandu après un avortement ou une fausse couche[12].
D'autres sources possibles de microchimérisme[modifier | modifier le code]
Un microchimérisme pourrait aussi suivre des transfusions sanguines faites à des patients gravement immunodéprimés ayant subi un traumatisme[13].
Lors de la gestation[14] le frère aîné, le frère jumeau ou le jumeau disparu d'un individu, peuvent avoir donné in utero quelques cellules à un autre embryon ou fœtus.
Animal[modifier | modifier le code]
Le microchimérisme au sein de paires de jumeaux est très courant chez les bovins. Chez les bovins (et autres Bovinés), les placentas des jumeaux fraternels fusionnent généralement et les jumeaux partagent la circulation sanguine, ce qui entraîne un échange de lignées cellulaires. Si les jumeaux sont une paire mâle-femelle, il en résulte un microchimérisme XX/XY et les hormones mâles masculinisent partiellement la génisse (femelle), créant une génisse martin ou freemartin. Les Freemartins semblent femelles, mais sont infertiles et ne peuvent donc pas être utilisées pour l'élevage ou la production laitière. Le microchimérisme fournit une méthode de diagnostic de la maladie, car le matériel génétique mâle peut être détecté dans un échantillon de sang[15].
Microchimérisme fœto-maternel dans le cerveau[modifier | modifier le code]
Plusieurs études ont trouvé de l'ADN masculin dans des cerveaux humains de mères après qu'elles ont porté un fœtus mâle (de même chez la souris)[16],[17].
Il a été suggéré que des cellules dérivées du fœtus pourraient se différencier en celles capables de présenter des immunomarqueurs neurotypiques à leur surface[16] Il n'y a aucune preuve solide pour dire que le microchimérisme du cerveau maternel conduit à la maladie, mais la maladie de Parkinson est corrélée à une incidence plus élevée de microchimères cérébrales[16]. Les études sur la maladie d'Alzheimer soutiennent presque la corrélation inverse : plus il y a de cellules dérivées du fœtus présentes, plus le risque que le patient ait eu la maladie d'Alzheimer est faible[17].
Tolérance maternelle aux antigènes paterno-fœtaux[modifier | modifier le code]
Il existe de nombreux mécanismes à l'interface mère-fœtus pour prévenir le rejet immunitaire des cellules fœtales. Des changements immunologiques systémiques surviennent pourtant chez la femme enceinte. Ainsi, l'état des femmes souffrant de maladies auto-immunes (par exemple polyarthrite rhumatoïde, sclérose en plaques) s'améliore le temps de la grossesse[18],[19]. Ces modifications des réponses immunitaires pendant la grossesse s'étendent aux composants maternels spécifiques aux antigènes fœtaux, en raison du transfert de cellules fœto-maternelles et de leur rétention dans les tissus maternels. A ce moment, le nombre de cellules fœtales dans les tissus maternels augmente et est en corrélation avec l'expansion des lymphocytes T régulateurs CD4+ (Tregs)[20]. La diminution de l'expansion et l'accumulation déciduale de Treg entraînent des complications pour la grossesse (prééclampsie, avortement)[20]. Dans le modèle murin, la plupart des lymphocytes T CD8+ spécifiques du fœtus de la mère subissent une délétion clonale[21] et expriment de faibles niveaux de récepteurs et de ligands de chimiokines, ce qui empêche les lymphocytes T CD8+ spécifiques du fœtus restants d'entrer dans l'interface mère-fœtus[22],[23]. Les cellules T CD4 + spécifiques au fœtus de la mère prolifèrent et, en raison de l'expression de FOXP3, se différencient en cellules Treg[24]. Chez la souris, les cellules Treg spécifiques du fœtus sont nécessaires pour une grossesse réussie[25].
Tolérance fœtale aux antigènes maternels non hérités[modifier | modifier le code]
Les lymphocytes T fœtaux s'accumulent au cours du développement in utero. Même si le fœtus est exposé à des « antigènes maternels non hérités » (NIMA pour les anglophones), les cellules T CD4 + fœtales sont capables de prolifération induite par alloantigène, se différenciant préférentiellement en cellules Treg et empêchant une réponse immunitaire fœtale aux antigènes maternels[26]. Cette tolérance immunitaire élargie persiste chez la mère et la progéniture après la naissance et permet aux cellules microchimériques d'être retenues dans les tissus.
Tolérance postnatale aux NIMA[modifier | modifier le code]
La tolérance spécifique au NIMA est à l'origine de certains phénotypes immunologiques intéressants : la sensibilisation aux antigènes du facteur Rhésus (Rh) érythrocytaire est réduite chez les femmes Rh- nées de femmes Rh+[27], la survie à long terme de l'allogreffe rénale est améliorée chez les paires de frères et sœurs donneur-receveur compatibles NIMA[28], ou l'acuité de la maladie du greffon contre l'hôte lors d'une greffe de moelle osseuse est réduite lorsque les receveurs de cellules souches du donneur sont compatibles NIMA[29]. Des études animales croisées montrent que lorsque l'exposition postnatale au NIMA par l'allaitement est éliminée, la survie des allogreffes compatibles avec le NIMA est réduite. Cela suggère que pour maintenir la tolérance spécifique au NIMA chez la progéniture, l'allaitement est essentiel, mais l'ingestion de cellules maternelles seules n'amorce pas la tolérance spécifique au NIMA. L'exposition prénatale et postnatale aux cellules de la mère est nécessaire pour maintenir la tolérance spécifique aux NIMA[30].
Avantages des cellules microchimériques[modifier | modifier le code]
Lors d'une grossesse, la gravité des troubles auto-immuns préexistants diminue, surtout quand les niveaux de cellules microchimériques fœtales sont les plus élevés - au cours du dernier trimestre[31],[19]. Ces cellules peuvent aussi remplacer les cellules maternelles blessées et permettre une récupération de la fonction tissulaire (chez la souris diabétique de type I, un remplacement de cellules défectueuses des îlots maternels par des cellules pancréatiques dérivées du fœtus a été observé)[32]. Les cellules microchimériques fœtales peuvent se différencier en types cellulaires qui infiltrent et remplacent les cellules lésées dans des modèles de maladie de Parkinson ou d'infarctus du myocarde. Elles aident les plaies à cicatriser (par néoangiogenèse).
L'ensemencement de cellules microchimériques fœtales dans les tissus maternels a été proposé pour promouvoir les soins de la progéniture après la naissance (l'ensemencement du tissu mammaire maternel peut favoriser la lactation et l'ensemencement du cerveau peut améliorer l'attention maternelle)[30].
Relation avec les maladies auto-immunes et le cancer du sein[modifier | modifier le code]
Le microchimérisme a été impliqué dans des maladies auto-immunes. Des études indépendantes ont suggéré que les cellules microchimériques d'origine fœtale pourraient être impliquées dans la pathogenèse de la sclérodermie systémique[3],[33]. Ces mêmes cellules pourraient être impliquées dans la pathogenèse d'un groupe de maladies auto-immunes de l'enfant : les myopathies inflammatoires idiopathiques juvéniles (un exemple serait la dermatomyosite juvénile)[34]. Le microchimérisme a maintenant été davantage impliqué dans d'autres maladies auto-immunes, notamment le lupus érythémateux disséminé[35].
Une hypothèse alternative sur le rôle des cellules microchimériques dans les lésions est qu'elles pourraient aussi faciliter la réparation tissulaire de l'organe endommagé[36].
Enfin, des cellules immunitaires fœtales sont souvent trouvées dans le stroma du cancer du sein par rapport aux échantillons prélevés chez des femmes en bonne santé. On ignore cependant si les lignées cellulaires fœtales favorisent le développement de tumeurs ou, au contraire, protègent les femmes contre le développement d'un cancer du sein[37],[38].
Le lupus érythémateux disséminé[modifier | modifier le code]
La présence de cellules fœtales chez les mères peut être associée à des avantages face à certaines maladies auto-immunes. En particulier, les cellules fœtales mâles sont liées à l'aide aux mères atteintes de lupus érythémateux disséminé.
Les femmes atteintes de néphrite lupique hébergeant des cellules fœtales mâles dans leurs biopsies rénales présentaient un meilleur fonctionnement du système rénal. Les taux de créatinine sérique, liés à l'insuffisance rénale, étaient faibles chez les mères présentant des taux élevés de cellules fœtales mâles[39]. En revanche, les femmes sans cellules fœtales mâles ayant une néphrite lupique présentaient une forme plus grave de glomérulonéphrite et des taux plus élevés de créatinine sérique[39].
Le rôle des cellules fœtales dans le microchimérisme lié à certaines maladies auto-immunes n'est pas bien compris.
Une hypothèse est qu'elles fournissent des antigènes, provoquant une inflammation et déclenchant la libération de différents antigènes étrangers[39]. Cela déclencherait une maladie auto-immune au lieu de guérir.
Une autre hypothèse est que les cellules microchimériques fœtales contribuent à la réparation des tissus. Lorsque les tissus deviennent enflammés, les cellules microchimériques fœtales se rendent sur le site endommagé et aident à la réparation et à la régénération des tissus[39].
Maladie thyroïdienne[modifier | modifier le code]
Le microchimérisme maternel fœtal peut être lié à des maladies thyroïdiennes auto-immunes. Des cellules fœtales ont parfois été trouvées dans le sang de muqueuse et dans les glandes thyroïdiennes de patients atteints de maladie thyroïdienne auto-immune ont été signalés. Ces cellules pourraient être activées après l'accouchement du bébé après la perte de l'immunosuppression chez la mère, ce qui suggère un rôle des cellules fœtales dans la pathogenèse de ces maladies[40].
Deux maladies thyroïdiennes, la thyroïdite de Hashimoto (HT) et la maladie de Graves (GD) présentent des similitudes avec la maladie du greffon contre l'hôte qui survient après une greffe de cellules souches hématopoïétiques. Les cellules fœtales colonisant les tissus maternels tels que la glande thyroïde sont capables de survivre de nombreuses années après l'accouchement.
Ces cellules microchimériques fœtales de la thyroïde apparaissent dans le sang des femmes atteintes de maladies thyroïdiennes[40].
Syndrome de Sjögren[modifier | modifier le code]
Le syndrome de Sjögren (SS) est une maladie rhumatismale auto-immune des glandes exocrines.
L'incidence accrue de SS après l'accouchement suggère une relation entre le SS et la grossesse, ce qui a conduit à l'hypothèse que le microchimérisme fœtal pourrait être impliqué dans la pathogenèse du SS.
On a trouvé des cellules fœtales positives au chromosome Y dans les glandes salivaires mineures chez 11 des 20 femmes atteintes de SS, mais chez un seul des huit témoins normaux, ce qui suggère qu'elles pourraient être impliquées dans le développement du SS[41].
Lichen plan oral[modifier | modifier le code]
Le lichen plan (LP) est une maladie chronique auto-immune médiée par les lymphocytes T d'étiologie inconnue. Sa prévalence est trois fois plus élevée chez la femme que chez l'homme.
Le LP est caractérisée par une infiltration de lymphocytes T dans les niveaux inférieurs de l'épithélium, où ils endommagent les cellules basales et provoquent l'apoptose. Le microchimérisme fœtal peut déclencher une réaction fœtus contre hôte et peut donc jouer un rôle dans la pathogenèse des maladies auto-immunes, y compris le LP[42].
Cancer du sein[modifier | modifier le code]
La grossesse semble améliorer le pronostic du cancer du sein[43],[44],[45] et augmenter les chances de survie après le diagnostic de cette maladie tumorale[46]. Ceci pourrait peut-être s'expliquer par la persistance de cellules fœtales dans le sang et les tissus maternels[2].
Les cellules fœtales migrent probablement activement du sang périphérique vers le tissu tumoral[47] où elles se fixent préférentiellement dans le stroma tumoral[38], et leur concentration diminue à mesure qu'elles se rapprochent du tissu mammaire sain[48]. Deux mécanismes suggérés par lesquels les cellules fœtales pourraient avoir un effet positif sur le pronostic du cancer du sein sont :
- les cellules fœtales ne « surveilleraient » que les cellules cancéreuses, et elles attireraient là, si nécessaire les composants du système immunitaire.
- La régulation à la baisse du système immunitaire induite par la présence de cellules fœtales pourrait finalement conduire à la prévention du cancer, car les femmes chez qui les CMF sont présentes produisent des taux plus faibles de médiateurs inflammatoires (qui conduisent au développement de tissu néoplasique)[49].
L'effet dépend aussi du niveau de microchimérisme : l'hyperchimérisme (degré de microchimérisme trop élevé) peut, au même titre que l'hypochimérisme (faible taux de microchimérisme), être lié à des effets négatif des CMF et ainsi favoriser un plus mauvais pronostic du cancer du sein[50],[51]. Les femmes atteintes d'un cancer du sein peuvent échouer dans le processus d'obtention et de maintien des cellules fœtales allogéniques. Une faible concentration et / ou une absence totale de cellules fœtales pourraient indiquer une prédisposition au développement du processus malin.
Autres cancers[modifier | modifier le code]
L'étude de S. Hallum montre une association entre les cellules fœtales d'origine masculine et le risque de cancer de l'ovaire. La présence du chromosome Y a été utilisée pour détecter les cellules étrangères dans le sang des femmes.
Le microchimérisme est le résultat de la grossesse, la possibilité que des cellules étrangères soient d'origine transfusionnelle ou de transplantation a été rejetée en raison de la santé des femmes.
Les femmes testées positives pour les cellules de microchimérisme d'origine masculine avaient des taux de risque de cancer de l'ovaire réduits par rapport aux femmes testées négatives[52]. La grossesse à un âge plus avancé peut réduire le risque de cancer de l'ovaire. Le nombre de cellules microchimériques diminue après la grossesse et le cancer de l'ovaire est plus fréquent chez les femmes ménopausées. Cela suggère que le microchimérisme fœtal pourrait avoir un rôle protecteur contre le cancer de l'ovaire. Les cellules microchimériques se regroupent également « plusieurs fois plus » dans les tumeurs pulmonaires que dans les tissus pulmonaires sains environnants. Les cellules fœtales de la moelle osseuse vont aux sites tumoraux où elles peuvent avoir des fonctions de réparation tissulaire[53]. Le microchimérisme d'origine du trafic de cellules fœto-maternelles pourrait être associé à la pathogenèse ou à la progression du cancer du col de l'utérus. Des cellules mâles ont été observées chez des patientes atteintes d'un cancer du col de l'utérus, mais pas chez des témoins positifs. Les cellules microchimériques pourraient induire l'altération du système immunitaire de la femme et rendre le tissu cervical plus sensible à l'infection par le VPH ou fournir un environnement propice à la croissance tumorale[54].
Rôle du microchimérisme dans la cicatrisation des plaies[modifier | modifier le code]
Des cellules fœtales microchimériques pouvant exprimer du collagène I, III et le TGF-β3, ont été identifiées dans des cicatrices de césarienne maternelles cicatrisées, suggèrent que ces cellules migrent vers le site des dommages dus aux signaux de lésions cutanées maternelles et aident à réparer les tissus[55].
Cellules souches[modifier | modifier le code]
Modèles animaux[modifier | modifier le code]
Le microchimérisme fœto-maternel a été démontré dans des études expérimentales visant à déterminer si les cellules fœtales peuvent traverser la barrière hémato-encéphalique chez la souris. Les propriétés de ces cellules leur permettent de traverser la barrière hémato-encéphalique et de cibler les tissus cérébraux lésés[56], car les cellules du sang du cordon ombilical expriment certaines protéines similaires aux neurones. Lorsque ces cellules sanguines du cordon ombilical sont injectées à des rats ayant subi une lésion cérébrale ou un accident vasculaire cérébral, elles pénètrent dans le cerveau et expriment certains marqueurs des cellules nerveuses. En raison de ce processus, les cellules fœtales pourraient pénétrer dans le cerveau pendant la grossesse et se différencier en cellules neurales. Le microchimérisme fœtal peut se produire dans le cerveau maternel de la souris, répondant à certains signaux dans le corps maternel[56].
Incidences sur la santé[modifier | modifier le code]
Le microchimérisme fœtal pourrait influencer la santé maternelle. L'isolement de cellules dans des cultures peut modifier les propriétés des cellules souches, mais pendant la grossesse, les effets des cellules souches fœtales peuvent être étudiés sans cultures in vitro. Une fois caractérisées et isolées, les cellules fœtales capables de traverser la barrière hémato-encéphalique pourraient avoir un impact sur certaines procédures[56]. Par exemple, l'isolement des cellules souches peut être réalisé en les prélevant à partir de sources telles que le cordon ombilical. Ces cellules souches fœtales peuvent être utilisées en perfusion intraveineuse pour réparer le tissu cérébral. Les changements hormonaux de la grossesse modifient la neurogenèse, ce qui pourrait créer des environnements favorables pour que les cellules fœtales réagissent aux blessures[56].
La véritable fonction des cellules fœtales chez les mères est mal connue, mais des effets positifs et négatifs sur la santé ont été signalés. Le partage de gènes entre le fœtus et la mère peut entraîner des avantages. Étant donné que tous les gènes ne sont pas partagés, des complications de santé peuvent survenir en raison de l'allocation des ressources[57]. Pendant la grossesse, les cellules fœtales sont capables de manipuler le système maternel pour tirer des ressources du placenta, tandis que le système maternel essaie de le limiter[57].
Notes et références[modifier | modifier le code]
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Microchimerism » (voir la liste des auteurs).
- (en) Sandhya Shrivastava, Rupali Naik, Hema Suryawanshi et Neha Gupta, « Microchimerism: A new concept », Journal of Oral and Maxillofacial Pathology, vol. 23, no 2, , p. 311 (ISSN 0973-029X, PMID 31516258, PMCID PMC6714269, DOI 10.4103/jomfp.JOMFP_85_17, lire en ligne, consulté le )
- (en) D. W. Bianchi, G. K. Zickwolf, G. J. Weil et S. Sylvester, « Male fetal progenitor cells persist in maternal blood for as long as 27 years postpartum. », Proceedings of the National Academy of Sciences, vol. 93, no 2, , p. 705–708 (PMID 8570620, PMCID 40117, DOI 10.1073/pnas.93.2.705, Bibcode 1996PNAS...93..705B).
- (en) Paul C. Evans, Nathalie Lambert, Sean Maloney et Dan E. Furst, « Long-Term Fetal Microchimerism in Peripheral Blood Mononuclear Cell Subsets in Healthy Women and Women With Scleroderma », Blood, vol. 93, no 6, , p. 2033–2037 (PMID 10068676, DOI 10.1182/blood.V93.6.2033.406k18_2033_2037).
- (en) « Comprehensive analysis of genes expressed by rare microchimeric fetal cells in the maternal mouse lung », Biology of Reproduction, vol. 87, no 2, , p. 42 (PMID 22674387, PMCID 3431427, DOI 10.1095/biolreprod.112.101147).
- (en) « Male microchimerism in the human female brain », PLOS ONE, vol. 7, no 9, , e45592 (PMID 23049819, PMCID 3458919, DOI 10.1371/journal.pone.0045592, Bibcode 2012PLoSO...745592C).
- Anne Kruchen, Tanja Stahl, Friederike Gieseke et Thomas MC Binder, « Fetomaternal Microchimerism Is Associated with Better Outcome in Haploidentical Hematopoietic Stem Cell Transplantation », Blood, vol. 124, no 21, , p. 1242 (DOI 10.1182/blood.V124.21.1242.1242).
- (en) « Maternal-fetal immunology and autoimmune disease: is some autoimmune disease auto-alloimmune or allo-autoimmune? », Arthritis and Rheumatism, vol. 39, no 2, , p. 191–4 (PMID 8849367, DOI 10.1002/art.1780390203).
- (en) « Transfer of fetal cells with multilineage potential to maternal tissue », JAMA, vol. 292, no 1, , p. 75–80 (PMID 15238593, DOI 10.1001/jama.292.1.75).
- (en) « Fetal microchimeric cells participate in tumour angiogenesis in melanomas occurring during pregnancy », The American Journal of Pathology, vol. 174, no 2, , p. 630–7 (PMID 19147820, PMCID 2630570, DOI 10.2353/ajpath.2009.080566).
- (en) « Fetal cells in maternal tissue following pregnancy: what are the consequences? », Human Reproduction Update, vol. 10, no 6, , p. 497–502 (PMID 15319378, DOI 10.1093/humupd/dmh040).
- (en) « Maternal microchimerism in healthy adults in lymphocytes, monocyte/macrophages and NK cells », Laboratory Investigation; A Journal of Technical Methods and Pathology, vol. 86, no 11, , p. 1185–92 (PMID 16969370, DOI 10.1038/labinvest.3700471).
- (en) « The influence of fetal loss on the presence of fetal cell microchimerism: a systematic review », Arthritis and Rheumatism, vol. 48, no 11, , p. 3237–41 (PMID 14613289, DOI 10.1002/art.11324).
- (en) « Transfusion-associated microchimerism: a new complication of blood transfusions in severely injured patients », Seminars in Hematology, vol. 44, no 1, , p. 24–31 (PMID 17198844, DOI 10.1053/j.seminhematol.2006.09.012).
- (en) R Shree, We Harrington, Sb Kanaan et A Forsyth, « Fetal microchimerism by mode of delivery: a prospective cohort study », BJOG, vol. 126, no 1, , p. 24–31 (PMID 30102819, PMCID 6294652, DOI 10.1111/1471-0528.15432).
- (en) A. Fujishiro, K. Kawakura, Y-I. Miyake et Y. Kaneda, « A fast, convenient diagnosis of the bovine freemartin syndrome using polymerase chain reaction », Theriogenology, vol. 43, no 5, , p. 883–891 (PMID 16727678, DOI 10.1016/0093-691X(95)00039-B).
- (en) Xiao Xia Zeng, Kian Hwa Tan, Ailing Yeo et Piriya, « Pregnancy-Associated Progenitor Cells Differentiate and Mature into Neurons in the Maternal Brain », Stem Cells and Development, vol. 19, no 12, , p. 1819–1830 (PMID 20707697, DOI 10.1089/scd.2010.0046).
- (en) « Male Microchimerism in the Human Female Brain », PLOS ONE, vol. 7, no 9, , e45592 (PMID 23049819, PMCID 3458919, DOI 10.1371/journal.pone.0045592, Bibcode 2012PLoSO...745592C, S2CID 8057434).
- (en) C Confavreux, M Hutchinson, MM Hours et P Cortinovis-Tourniaire, « Rate of pregnancy-related relapse in multiple sclerosis. Pregnancy in Multiple Sclerosis Group. », The New England Journal of Medicine, vol. 339, no 5, , p. 285–91 (PMID 9682040, DOI 10.1056/NEJM199807303390501).
- (en) Monika Østensen et Peter M. Villiger, « The remission of rheumatoid arthritis during pregnancy », Seminars in Immunopathology, vol. 29, no 2, , p. 185–191 (PMID 17621703, DOI 10.1007/s00281-007-0072-5, S2CID 5766992, lire en ligne).
- (en) Tony T. Jiang, Vandana Chaturvedi, James M. Ertelt et Jeremy M. Kinder, « Regulatory T Cells: New Keys for Further Unlocking the Enigma of Fetal Tolerance and Pregnancy Complications », The Journal of Immunology, vol. 192, no 11, , p. 4949–4956 (PMID 24837152, PMCID 4030688, DOI 10.4049/jimmunol.1400498).
- (en) A Erlebacher, D Vencato, KA Price et D Zhang, « Constraints in antigen presentation severely restrict T cell recognition of the allogeneic fetus. », The Journal of Clinical Investigation, vol. 117, no 5, , p. 1399–411 (PMID 17446933, PMCID 1849983, DOI 10.1172/JCI28214).
- (en) Vandana Chaturvedi, James M. Ertelt, Tony T. Jiang et Jeremy M. Kinder, « CXCR3 blockade protects against Listeria monocytogenes infection–induced fetal wastage », Journal of Clinical Investigation, vol. 125, no 4, , p. 1713–1725 (PMID 25751061, PMCID 4396484, DOI 10.1172/JCI78578).
- (en) P. Nancy, E. Tagliani, C.-S. Tay et P. Asp, « Chemokine Gene Silencing in Decidual Stromal Cells Limits T Cell Access to the Maternal-Fetal Interface », Science, vol. 336, no 6086, , p. 1317–1321 (PMID 22679098, PMCID 3727649, DOI 10.1126/science.1220030, Bibcode 2012Sci...336.1317N).
- (en) Jared H. Rowe, James M. Ertelt, Lijun Xin et Sing Sing Way, « Pregnancy imprints regulatory memory that sustains anergy to fetal antigen », Nature, vol. 490, no 7418, , p. 102–106 (PMID 23023128, PMCID 3465465, DOI 10.1038/nature11462, Bibcode 2012Natur.490..102R).
- (en) Lijun Xin, James M. Ertelt, Jared H. Rowe et Tony T. Jiang, « Cutting Edge: Committed Th1 CD4 + T Cell Differentiation Blocks Pregnancy-Induced Foxp3 Expression with Antigen-Specific Fetal Loss », The Journal of Immunology, vol. 192, no 7, , p. 2970–2974 (PMID 24591368, PMCID 3972488, DOI 10.4049/jimmunol.1302678).
- (en) Jeff E. Mold, Jakob Michaëlsson, Trevor D. Burt et Marcus O. Muench, « Maternal Alloantigens Promote the Development of Tolerogenic Fetal Regulatory T Cells in Utero », Science, vol. 322, no 5907, , p. 1562–1565 (PMID 19056990, PMCID 2648820, DOI 10.1126/science.1164511, Bibcode 2008Sci...322.1562M).
- (en) Ray D. Owen, Harold R. Wood, Alvin G. Foord et Phillip Sturgeon, « Evidence for actively acquired tolerance to Rh antigens », Proceedings of the National Academy of Sciences of the United States of America, vol. 40, no 6, , p. 420–424 (PMID 16589498, PMCID 534062, DOI 10.1073/pnas.40.6.420, Bibcode 1954PNAS...40..420O).
- (en) William J. Burlingham, Alan P. Grailer, Dennis M. Heisey et Frans H.J. Claas, « The Effect of Tolerance to Noninherited Maternal HLA Antigens on the Survival of Renal Transplants from Sibling Donors », New England Journal of Medicine, vol. 339, no 23, , p. 1657–1664 (PMID 9834302, DOI 10.1056/NEJM199812033392302).
- (en) J. J. van Rood, FR Loberiza, MJ Zhang et M Oudshoorn, « Effect of tolerance to noninherited maternal antigens on the occurrence of graft-versus-host disease after bone marrow transplantation from a parent or an HLA-haploidentical sibling », Blood, vol. 99, no 5, , p. 1572–1577 (PMID 11861270, DOI 10.1182/blood.v99.5.1572).
- (en) Jeremy M. Kinder, Ina A. Stelzer, Petra C. Arck et Sing Sing Way, « Immunological implications of pregnancy-induced microchimerism », Nature Reviews. Immunology, vol. 17, no 8, , p. 483–494 (PMID 28480895, PMCID 5532073, DOI 10.1038/nri.2017.38).
- (en) Christian Confavreux, Michael Hutchinson, Martine Marie Hours et Patricia Cortinovis-Tourniaire, « Rate of Pregnancy-Related Relapse in Multiple Sclerosis », New England Journal of Medicine, vol. 339, no 5, , p. 285–291 (PMID 9682040, DOI 10.1056/NEJM199807303390501).
- (en) Rei Sunami, Mayuko Komuro, Tsutomu Yuminamochi et Kazuhiko Hoshi, « Fetal cell microchimerism develops through the migration of fetus-derived cells to the maternal organs early after implantation », Journal of Reproductive Immunology, vol. 84, no 2, , p. 117–123 (PMID 20116109, DOI 10.1016/j.jri.2009.11.006).
- (en) Carol M. Artlett, J. Bruce Smith et Sergio A. Jimenez, « Identification of Fetal DNA and Cells in Skin Lesions from Women with Systemic Sclerosis », New England Journal of Medicine, vol. 338, no 17, , p. 1186–1191 (PMID 9554859, DOI 10.1056/NEJM199804233381704, lire en ligne).
- (en) « Chimeric cells of maternal origin in juvenile idiopathic inflammatory myopathies. Childhood Myositis Heterogeneity Collaborative Group », Lancet, vol. 356, no 9248, , p. 2155–6 (PMID 11191545, DOI 10.1016/S0140-6736(00)03499-1, S2CID 46327174).
- (en) « Microchimerism in a female patient with systemic lupus erythematosus », Arthritis and Rheumatism, vol. 44, no 9, , p. 2107–11 (PMID 11592373, DOI 10.1002/1529-0131(200109)44:9<2107::AID-ART361>3.0.CO;2-9).
- (en) « Microchimerism and skin disease: true-true unrelated? », The Journal of Investigative Dermatology, vol. 126, no 2, , p. 239–41 (PMID 16418731, DOI 10.1038/sj.jid.5700061).
- (en) « Fetal microchimerism in women with breast cancer », Cancer Research, vol. 67, no 19, , p. 9035–8 (PMID 17909006, DOI 10.1158/0008-5472.CAN-06-4209).
- (en) Gil Dubernard, Sélim Aractingi, Michel Oster et Roman Rouzier, « Breast cancer stroma frequently recruits fetal derived cells during pregnancy », Breast Cancer Research, vol. 10, no 1, , R14 (PMID 18271969, PMCID 2374970, DOI 10.1186/bcr1860).
- (en) « Fetal microchimerism in kidney biopsies of lupus nephritis patients may be associated with a beneficial effect », Arthritis Research & Therapy, vol. 17, , p. 101 (PMID 25889410, PMCID 4416327, DOI 10.1186/s13075-015-0615-4).
- (en) « Fetal microchimeric cells in autoimmune thyroid diseases: harmful, beneficial or innocent for the thyroid gland? », Chimerism, vol. 4, no 4, , p. 111–8 (PMID 23723083, PMCID 3921191, DOI 10.4161/chim.25055).
- (en) Y. Endo, I Negishi et O Ishikawa, « Possible contribution of microchimerism to the pathogenesis of Sjogren's syndrome », Rheumatology, vol. 41, no 5, , p. 490–495 (PMID 12011370, DOI 10.1093/rheumatology/41.5.490).
- Sandhya Shrivastava, Rupali Naik, Hema Suryawanshi et Neha Gupta, « Microchimerism: A new concept », Journal of Oral and Maxillofacial Pathology, vol. 23, no 2, , p. 311 (PMID 31516258, PMCID 6714269, DOI 10.4103/jomfp.JOMFP_85_17).
- (en) « Childbirth and breast cancer prognosis », International Journal of Cancer, vol. 111, no 5, , p. 772–6 (PMID 15252849, DOI 10.1002/ijc.20323, S2CID 8782090).
- (en) Sara H. Olson, Ann G. Zauber, Jian Tang et Susan Harlap, « Relation of Time since Last Birth and Parity to Survival of Young Women with Breast Cancer », Epidemiology, vol. 9, no 6, , p. 669–671 (PMID 9799180, DOI 10.1097/00001648-199811000-00019).
- (en) Penny R. Anderson, Alexandra L. Hanlon, Gary M. Freedman et Nicos Nicolaou, « Parity Confers Better Prognosis in Older Women with Early-Stage Breast Cancer Treated with Breast-Conserving Therapy », Clinical Breast Cancer, vol. 5, no 3, , p. 225–231 (PMID 15335456, DOI 10.3816/cbc.2004.n.026).
- (en) « Reproductive factors and histologic subtype in relation to mortality after a breast cancer diagnosis », Breast Cancer Research and Treatment, vol. 130, no 3, , p. 975–80 (PMID 21769659, PMCID 4306414, DOI 10.1007/s10549-011-1666-0).
- (en) « Increased fetal cell microchimerism in high grade breast carcinomas occurring during pregnancy », International Journal of Cancer, vol. 124, no 5, , p. 1054–9 (PMID 19065666, DOI 10.1002/ijc.24036, S2CID 29640302).
- (en) « Heterogeneous Distribution of Fetal Microchimerism in Local Breast Cancer Environment », PLOS ONE, vol. 11, no 1, , e0147675 (PMID 26808509, PMCID 4726590, DOI 10.1371/journal.pone.0147675, Bibcode 2016PLoSO..1147675N).
- (en) « Inflammation and cancer », Nature, vol. 420, no 6917, , p. 860–7 (PMID 12490959, PMCID 2803035, DOI 10.1038/nature01322, Bibcode 2002Natur.420..860C).
- (en) « Case-control study of fetal microchimerism and breast cancer », PLOS ONE, vol. 3, no 3, , e1706 (PMID 18320027, PMCID 2248618, DOI 10.1371/journal.pone.0001706, Bibcode 2008PLoSO...3.1706G).
- (en) « High male chimerism in the female breast shows quantitative links with cancer », International Journal of Cancer, vol. 133, no 4, , p. 835–42 (PMID 23390035, DOI 10.1002/ijc.28077, S2CID 23272121).
- (en) Sara Hallum, Marianne Antonius Jakobsen, Thomas Alexander Gerds et Anja Pinborg, « Male origin microchimerism and ovarian cancer », International Journal of Epidemiology, vol. 50, no 1, , p. 87–94 (ISSN 0300-5771, PMID 32065627, DOI 10.1093/ije/dyaa019).
- (en) J. A. Sawicki, « Fetal Microchimerism and Cancer », Cancer Research, vol. 68, no 23, , p. 9567–9569 (PMID 19047129, PMCID 2638004, DOI 10.1158/0008-5472.CAN-08-3008).
- (en) D Cha, « Cervical cancer and microchimerism », Obstetrics & Gynecology, vol. 102, no 4, , p. 774–781 (PMID 14551008, DOI 10.1016/S0029-7844(03)00615-X).
- (en) Uzma Mahmood et Keelin O’Donoghue, « Microchimeric fetal cells play a role in maternal wound healing after pregnancy », Chimerism, vol. 5, no 2, , p. 40–52 (PMID 24717775, PMCID 4199806, DOI 10.4161/chim.28746).
- (en) « Fetal microchimerism in the maternal mouse brain: a novel population of fetal progenitor or stem cells able to cross the blood-brain barrier? », Stem Cells, vol. 23, no 10, , p. 1443–52 (PMID 16091558, DOI 10.1634/stemcells.2004-0169, S2CID 37875663).
- (en) « Fetal microchimerism and maternal health: a review and evolutionary analysis of cooperation and conflict beyond the womb », BioEssays, vol. 37, no 10, , p. 1106–18 (PMID 26316378, PMCID 4712643, DOI 10.1002/bies.201500059).
Voir aussi[modifier | modifier le code]
Bibliographie[modifier | modifier le code]
- (en) Sandhya Shrivastava, Rupali Naik, Hema Suryawanshi et Neha Gupta, « Microchimerism. A new concept », Journal of Oral and Maxillofacial Pathology (en), vol. 23, no 2, , p. 311- (DOI 10.4103/jomfp.JOMFP_85_17
 )
)
Articles connexes[modifier | modifier le code]
Liens externes[modifier | modifier le code]
- Ressource relative à la santé :
- Notice dans un dictionnaire ou une encyclopédie généraliste :