Méthacrylamide

| Méthacrylamide | |
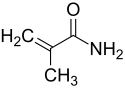 | |
| Structure du méthacrylamide | |
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.001.094 |
| No CE | 201-202-3 |
| No RTECS | UC6475000 |
| PubChem | 6595 |
| ChEBI | 51759 |
| Apparence | solide combustible incolore cristallisé, inodore et peu inflammable, très soluble dans l'eau[1] |
| Propriétés chimiques | |
| Formule | C4H7NO [Isomères] C4H7NO |
| Masse molaire[2] | 85,104 5 ± 0,004 2 g/mol C 56,45 %, H 8,29 %, N 16,46 %, O 18,8 %, 85.106 |
| Propriétés physiques | |
| T° fusion | 106 à 109 °C[1] |
| T° ébullition | 215 °C[1] |
| Solubilité | 202 g/L[1] à 20 °C |
| Masse volumique | 1,10 à 1,12 g/cm3[1] à 20 °C |
| T° d'auto-inflammation | 510 °C[1] |
| Limites d’explosivité dans l’air | à partir de 15 g/m3[1] |
| Précautions | |
| SGH[1] | |
| H302, H319, H335, H371, H373, P260, P264, P270 et P271 | |
| NFPA 704[3] | |
| Écotoxicologie | |
| DL50 | 459 mg/kg[1] (souris, oral) |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier | |
Le méthacrylamide est un composé chimique de formule CH2=C(CH3)CONH2. Il se présente sous la forme d'un solide combustible incolore cristallisé, inodore et peu inflammable, très soluble dans l'eau, sensible à la lumière et susceptible de polymériser. Il se décompose au-dessus de 106 à 109 °C en libérant des oxydes d'azote.
Il est obtenu par hydrolyse de la cyanhydrine d'acétone (CH3)2C(OH)C≡N par l'acide sulfurique H2SO4[4].
Le méthacrylamide est utilisé comme monomère pour produire des polymères (granulés acryliques, par exemple pour les peintures thermodurcissables et les dispersions auto-réticulables, ou encore des hydrogels[5]) et pour produire du méthacrylate de méthyle CH2=C(CH3)COOCH3[6].
Notes et références[modifier | modifier le code]
- Entrée « Methacrylamide » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 17 avril 2022 (JavaScript nécessaire)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « Fiche du composé Methacrylamide, 98% », sur Alfa Aesar (consulté le ).
- (en) Richard H. Wiley et Walter E. Waddey, « Methacrylamide », Organic Syntheses, vol. 29, , p. 61 (DOI 10.15227/orgsyn.029.0061, lire en ligne)
- (en) Vladimir A. Kornev, Ekaterina A. Grebenik, Anna B. Solovieva, Ruslan I. Dmitrieva et Peter S. Timashev, « Hydrogel-assisted neuroregeneration approaches towards brain injury therapy: A state-of-the-art review », Computational and Structural Biotechnology Journal, vol. 16, , p. 488-502 (PMID 30455858, PMCID 6232648, DOI 10.1016/j.csbj.2018.10.011, lire en ligne)
- (en) Koichi Nagai, « New developments in the production of methyl methacrylate », Applied Catalysis A: General, vol. 221, nos 1-2, , p. 367-377 (DOI 10.1016/S0926-860X(01)00810-9, lire en ligne)


