Valoración complexométrica

Valoración complexométrica (o Quelatometría) es una forma de análisis volumétrico basado en la formación de compuestos poco disociados:[1] halogenuros de mercurio, cianuro de plata, fluoruro de aluminio. Se suele utilizar la formación de un complejo coloreado para indicar el punto final de la valoración. Las valoraciones complexométricas son particularmente útiles para la determinación de una mezcla de diferentes iones metálicos en solución. Generalmente se utiliza un indicador capaz de producir un cambio de color nítido para detectar el punto final de la valoración.
Reacciones para valoración complexométrica[editar]
En teoría, cualquier reacción de complejación se puede utilizar como una técnica volumétrica, siempre que:
- la reacción alcanza el equilibrio rápidamente después de que se añade cada porción de valorante.
- no se plantean situaciones interferentes. Por ejemplo, la formación gradual de varios complejos diferentes del ion metálico con el valorante, dando como resultado la presencia de más de un complejo en solución durante el proceso de valoración.
- se disponga de un indicador complexométrico capaz de localizar el punto de equivalencia con bastante exactitud.
Mercurimetría[editar]
El catión Hg2+ forma un gran número de compuestos poco disociados (con F-, Cl-, I- y SCN-). Estos iones se pueden valorar con una disolución de Hg2+ utilizando un indicador adecuado. Los cloruros pueden valorarse con Hg2+ según la reacción:
- Hg2+ + 2 Cl- → HgCl2
El HgCl2 está disociado menos del 1% en disolución 0,1 M. Como indicador se utiliza nitroprusiato de sodio, Na2(Fe(CN)5NO), en cantidad de 1 mL de disolución de indicador al 10% por cada 100 mL de disolución. Cuando se alcanza el punto de equivalencia, se forma nitroprusiato de mercurio, Hg(Fe(CN)5NO), poco soluble. A menudo es necesario una cierta corrección del efecto del indicador. Los iones que precipitan con el nitroprusiato perturban la valoración: (Cu2+, Co2+, Ni2+), así como los que forman complejos con el Hg2+.
También puede emplearse como indicador difenilcarbacida (pH óptimo entre 1,5-2,0) o difenilcarbazona (pH óptimo entre 3,2-3,3) junto con bromofenol para ajustar el pH y que dan coloración violeta con el Hg2+.
Los bromuros se valoran igual que los cloruros.
Los ioduros se valoran mediante la reacción:
- Hg2+ + 4 l- → Hgl42-
En el punto de equivalencia un pequeño exceso de Hg2+ produce la formación de HgI2, precipitado insoluble de color rojo.
Los sulfocianuros se valoran (en medio nítrico) según la reacción:
- 2 SCN- + Hg2+ → Hg(SCN)2
Argentometría[editar]
El catión Ag+ forma un complejo con el ion cianuro (CN-) lo que sirve para su valoración, según la ecuación:
- 2 CN- + Ag+ → Ag(CN)2-
Cuando se alcanza el punto final aparece una turbidez blanca (técnica de Liebig):
- Ag(CN)2- + Ag+ → Ag(CN)2Ag
Valoración complexométrica con EDTA[editar]
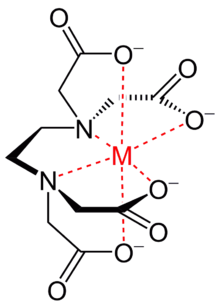
El ácido etilendiaminotetraacético (EDTA o AEDT), tiene cuatro grupos carboxilo y dos grupos amino que pueden actuar como donantes de pares de electrones, o bases de Lewis. La capacidad del EDTA para potencialmente donar hasta sus seis pares de electrones libres, para la formación de enlaces covalentes coordinados, a los cationes metálicos hace del EDTA un ligando hexadentado. Sin embargo, en la práctica el EDTA está, por lo general, sólo parcialmente ionizado, y por lo tanto forma menos de seis enlaces covalentes coordinados con los cationes metálicos.
El EDTA disódico se utiliza comúnmente para estandarizar las soluciones acuosas de cationes metálicos de transición. El EDTA disódico (a veces escrito como Na2H2Y) sólo forma cuatro enlaces covalentes coordinados con los cationes metálicos a valores de pH ≤ 12. En este rango de pH, los grupos amino permanecen protonados y por lo tanto no pueden donar electrones para la formación de enlaces covalentes coordinados. Tengase en cuenta que la forma abreviada Na4-xHxY puede utilizarse para representar una especie de EDTA, donde x designa el número de protones ácidos unidos a la molécula de EDTA.
El EDTA forma un complejo octaédrico con la mayoría de los cationes metálicos divalentes, M2+, en solución acuosa. La principal razón de que el EDTA se utilice tan ampliamente en la estandarización de soluciones de cationes metálicos es que la constante de formación de la mayoría de los complejos catión metálico-EDTA es muy alta, lo que significa que el equilibrio de la reacción:
- M2+ + H4Y → MH2Y + 2H+
se encuentra muy desplazado hacia la derecha. Llevar a cabo la reacción en una solución tampón básica elimina los H+, conforme se van formando, lo que también favorece la formación del producto de reacción catión metálico-EDTA. Para la mayoría de los propósitos que se puede considerar que la formación del complejo catión metálico-EDTA es completa, y es por esto por lo que el EDTA se utiliza en las valoraciones / estandarizaciones de este tipo.
Para llevar a cabo las valoraciones de cationes metálicos utilizando EDTA, casi siempre es necesario utilizar un indicador complexométrico para determinar cuándo se ha alcanzado el punto final. Los indicadores más comunes son colorantes orgánicos como el Negro sulfónico, Negro de eriocromo T, Rojo de eriocromo B o Murexida. Estos colorantes se unen a los cationes metálicos en solución para formar complejos coloreados. Sin embargo, como el EDTA se une a los cationes metálicos mucho más fuertemente que al colorante utilizado como indicador, el EDTA se desplaza el colorante de los cationes metálicos de la solución analito. Un cambio de color en la solución que está siendo valorada indica que todo el colorante ha sido desplazado de los cationes metálicos en solución, y que se ha alcanzado el punto final. De esta forma, el indicador libre (más que el complejo metálico) sirve como indicador de punto final.
La Trietanolamina también se utiliza como un agente complejante para enmascarar otros cationes, como los iones de aluminio, en solución acuosa antes de realizar una valoración de complexométrica. Múltiples iones metálicos pueden ser valorados secuencialmente mediante un cuidadoso control del pH.
Referencias[editar]
- ↑ Pino, F., Varcarcel M. (1978), Equilibrios iónicos en disolución. Análisis volumétrico.
Véase también[editar]
Enlaces externos[editar]
- Esta obra contiene una traducción derivada de «Complexometric titration» de Wikipedia en inglés, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.