Pseudotropin
 Van Wikipedia, de gratis encyclopedie
Van Wikipedia, de gratis encyclopedie
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
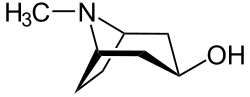 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Pseudotropin | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C8H15NO | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 141,21 g·mol−1 | ||||||||||||||||||
| Aggregatzustand | fest[1] | ||||||||||||||||||
| Dichte | 0,998 g·cm−3 (bei 116 °C)[1] | ||||||||||||||||||
| Schmelzpunkt | 109 °C[1] | ||||||||||||||||||
| Siedepunkt | 241 °C[1] | ||||||||||||||||||
| Löslichkeit | löslich in Wasser[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Pseudotropin ist eine chemische Verbindung aus der Gruppe der Tropanole und ein Isomer von Tropin.
Vorkommen[Bearbeiten | Quelltext bearbeiten]
Pseudotropin kann zusammen mit mehreren anderen Alkaloiden in der Koka-Pflanze gefunden werden.[2] Daneben kommt es auch im weißen Bilsenkraut[3] und in der Tollkirsche[4] vor.
- Koka-Pflanze
- Tollkirsche
Biosynthese[Bearbeiten | Quelltext bearbeiten]
In Nachtschattengewächsen konnte gezeigt werden, dass Tropin und Pseudotropin beide NADPH-abhängige Reduktion von Tropinon entstehen, wobei die beiden Produkte durch zwei Enzyme gebildet werden.[4]
Herstellung[Bearbeiten | Quelltext bearbeiten]
Pseudotropin fällt bei der Reduktion von Tropinon neben Tropin an. Da das Pseudotropin gegenüber Tropin stabiler ist, kann ersteres auch durch Epimerisierung gewonnen werden, indem letzteres mit Natriumpentanolat[S 1] gekocht wird.[5]
Eine Totalsynthese ist ausgehend von 4-Nitro-1-buten[S 2] möglich. Dieses wird zunächst mit Acrolein und Natriummethanolat in Methanol zu einem Acetal umgesetzt. Durch Reduktion mit Zink und Ammoniumchlorid wird ein monocyclisches Nitron erhalten, das durch Erhitzen in Toluol am Rückfluss zu einem Tricyclus cyclisiert werden kann. Die Struktur dieses Intermediats entspricht im Wesentlichen dem Pseudotropin, es enthält jedoch eine zusätzliche Bindung zwischen Stickstoff und Sauerstoff und es weist keine N-Methylgruppe auf. Die Verbindung kann auch leicht in Pseudotropin umgewandelt werden: Entweder durch Hydrierung an Palladium und anschließende Methylierung mittels Eschweiler-Clarke-Reaktion oder durch Methylierung mit Methyliodid und anschließende Reduktion mit Lithiumaluminiumhydrid.[6]
Reaktionen[Bearbeiten | Quelltext bearbeiten]
Die Oxidation von Pseudotropin ergibt Tropinon, die Dehydratisierung Tropidin.[5][S 3]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e f g Datenblatt Pseudotropin bei Sigma-Aldrich, abgerufen am 17. April 2024 (PDF).
- ↑ Amy Sue Biondich, Jeremy David Joslin: Coca: The History and Medical Significance of an Ancient Andean Tradition. In: Emergency Medicine International. Band 2016, 2016, S. e4048764, doi:10.1155/2016/4048764, PMID 27144028, PMC 4838786 (freier Volltext).
- ↑ Katja Doerk-Schmitz, Ludger Witte, A.Wilhelm Alfermann: Tropane alkaloid patterns in plants and hairy roots of Hyoscyamus albus. In: Phytochemistry. Band 35, Nr. 1, Dezember 1993, S. 107–110, doi:10.1016/S0031-9422(00)90517-X.
- ↑ a b B. Dräger, A. Schaal: Isolation of Pseudotropine-Forming Tropinone Reductase from Atropa belladonna Root Cultures. In: Planta Medica. Band 57, S 2, Dezember 1991, S. A99–A100, doi:10.1055/s-2006-960382.
- ↑ a b Alex Nickon, Louis F. Fieser: Configuration of Tropine and Pseudotropine. In: Journal of the American Chemical Society. Band 74, Nr. 22, November 1952, S. 5566–5570, doi:10.1021/ja01142a005.
- ↑ Joseph J. Tufariello, George B. Mullen, John J. Tegeler, Eugene J. Trybulski, Shing Chun Wong, S. Asrof Ali: Synthesis in the tropane class of alkaloids. Pseudotropine and dl-cocaine. In: Journal of the American Chemical Society. Band 101, Nr. 9, April 1979, S. 2435–2442, doi:10.1021/ja00503a033.
Anmerkungen[Bearbeiten | Quelltext bearbeiten]
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Natriumpentanolat: CAS-Nummer: 1941-84-0, PubChem: 23675634, Wikidata: Q125547553.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 4-Nitro-1-buten: CAS-Nummer: 32349-29-4, PubChem: 10887842, Wikidata: Q82265862.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Tropidin: CAS-Nummer: 529-18-0, PubChem: 564942, Wikidata: Q125547560.


