Humanes Herpesvirus 6
 Van Wikipedia, de gratis encyclopedie
Van Wikipedia, de gratis encyclopedie
| Humanes Herpesvirus 6A und 6B | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
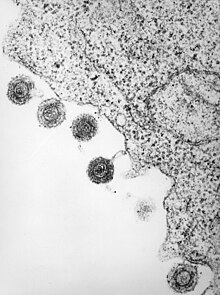
 HHV-6 Viruspartikel unter dem Elektronenmikroskop. | ||||||||||||||||||||||
| Systematik | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Wissenschaftlicher Name | ||||||||||||||||||||||
| Human betaherpesvirus 6A/6B | ||||||||||||||||||||||
| Kurzbezeichnung | ||||||||||||||||||||||
| HHV-6A, HHV-6B | ||||||||||||||||||||||
| Links | ||||||||||||||||||||||
|

Das Humane Herpesvirus Typ 6A und 6B (HHV-6A und 6B) sind zwei humanpathogene Viren (Spezies Roseolovirus humanbeta6a und R. humanbeta6b) aus der Unterfamilie der Betaherpesviren (Betaherpesvirinae) in der Familie Herpesviridae. Das International Committee on Taxonomy of Viruses (ICTV) hat die frühere Virusspezies (Humanes) Herpesvirus 6 mit Stand März 2019 aufgeteilt und die beiden Subtypen A und B in den Rang von Spezies erhoben.[2]
HHV-6B ist der Verursacher des Drei-Tage-Fiebers (Exanthema subitum alias Roseola infantum, „Sechste Krankheit“), einer Erkrankung, die vorwiegend im Säuglings- oder frühen Kleinkindalter auftritt. Mit HHV-6A konnten bisher keine Erkrankungen assoziiert werden. Eine Beteiligung dieser Viren an anderen Erkrankungen wird diskutiert (s. u.).
Historisches[Bearbeiten | Quelltext bearbeiten]
HHV-6A wurde 1986 in der Arbeitsgruppe von Robert Gallo am NIH entdeckt.[3] Die Entdecker glaubten, es mit einem B-Zell-lymphotropen Herpesvirus zu tun zu haben (daher das veraltete Acronym HBLV). Bald stellte sich aber heraus, dass HHV-6 CD4-positive T-Lymphozyten infiziert. HHV-6 ist damit neben dem später entdeckten Humanen Herpesvirus Typ 7 das einzige bisher bekannte humane Herpesvirus, das primär T-Lymphozyten infiziert (alle anderen humanen Herpesviren sind B-Zell-lymphotrop).
Epidemiologie und Übertragung[Bearbeiten | Quelltext bearbeiten]
HHV-6A/B sind praktisch ubiquitär verbreitete Viren. Im Erwachsenenalter sind mindestens 80 % der Bevölkerung seropositiv, das heißt latent mit einem der Viren infiziert (wenn auch nicht unbedingt erkrankt). Die Infektion geschieht dabei meist im Säuglings- oder Kleinkindalter durch Tröpfcheninfektion und verläuft häufig klinisch inapparent, das heißt ohne wesentliche Symptome. Die symptomatische Infektion äußert sich meist als Drei-Tage-Fieber.
Latenz[Bearbeiten | Quelltext bearbeiten]
Wie alle Herpesviren besitzen HHV-6A und -6B die Fähigkeit zur „Latenz“, das heißt zum „Überdauern“ im Organismus über lange Zeit. In der Regel kann das Virus nach Infektion nicht mehr vollständig eliminiert werden. Meist verursacht es keine weiteren Probleme, es kann jedoch wiederaufleben und sich erneut vermehren, wenn das Immunsystem geschwächt ist.
HHV-6-Enzephalitis[Bearbeiten | Quelltext bearbeiten]
Bei immunsupprimierten Patienten und insbesondere nach allogener Stammzelltransplantation ist das HHV-6B eine der häufigsten Ursachen einer Enzephalitis. Dabei kommt es zu einer Reaktivierung einer chronisch-latenten HHV-6B-Infektion, die bei 30–70 % der Stammzelltransplantierten nachweisbar ist. Die Inzidenz einer HHV-6-Enzephalitis nach Stammzelltransplantation liegt bei 1,4 %, aber 98 % aller Enzephalitiden nach Stammzelltransplantation sind auf HHV-6B zurückzuführen. Als Risikofaktoren für eine Reaktivierung gelten ein HLA-Mismatch, eine T-Zelldepletion und eine Cortison-Therapie. Weiterhin haben 90 % aller Patienten mit HHV-6-Enzephalitis Nabelschnurblutstammzellen erhalten.
Die Enzephalitis ist selten fulminant, sondern meist subakut, langsam beginnend und äußert sich anfangs oft durch Verwirrtheit, dazu können eine anterograde Amnesie, Persönlichkeitsänderungen, Irritabilität und epileptische Anfälle kommen. Fieber ist selten. Im Liquor zeigt sich oft eine leichte Leukozytose, vor allem als Lymphozytose und mit erhöhtem Proteinspiegel. Ein Virusnachweis ist im Liquor möglich. In der Kernspintomographie finden sich ebenfalls meist keine spezifischen Veränderungen, selten können aber Läsionen in der Amygdala oder im Hippocampus gefunden werden.
Erste Symptome können zwei bis sechs Wochen nach der Stammzelltransplantation auftreten, aber auch Latenzen bis zwanzig Wochen nach der Transplantation wurden beobachtet.
Die antivirale Behandlung ist empirisch, es liegen nur Beobachtungsstudien vor. Erste Wahl ist Foscarnet, alternativ oder zusätzlich kann Ganciclovir eingesetzt werden, während Cidofovir wegen des hohen Risikos von Nierenschädigungen eher vermieden wird. Da auch diese beiden Mittel mit schweren unerwünschten Wirkungen verbunden sind, u. a. Nierenschädigungen, Knochenmarksuppression, Elektrolytänderungen und epileptische Anfälle, muss eine engmaschige Überwachung stattfinden.[4]
Virusnachweis[Bearbeiten | Quelltext bearbeiten]
Der Virusnachweis gelingt in der Regel serologisch, das heißt durch den Nachweis von Antikörpern gegen das Virus. Diese werden jedoch erst einige Zeit nach der Infektion gebildet. Bei Säuglingen können auch noch durch die Mutter über die Plazenta übertragene Antikörper vorhanden sein, die das Bild verfälschen können. In der Phase der akuten Infektion lässt sich die Virus-DNA mittels Polymerase-Kettenreaktion (PCR) oder elektronenmikroskopisch nachweisen. Neben dem Nachweis im peripheren Blut gelingt dieser bei Menschen mit einer geerbten chromosomalen integrierten HHV6-Infektion in jeder Körperzelle.
Therapie und Impfung[Bearbeiten | Quelltext bearbeiten]
Eine Impfung gegen HHV-6B steht bisher nicht zur Verfügung. Bei schwerwiegenden Komplikationen (z. B. Enzephalitis) sollte eine antivirale Therapie mit Ganciclovir oder Foscarnet versucht werden. Größere Studien, die die Wirksamkeit dieser Virostatika belegen würden, gibt es aber bisher nicht.
HHV-6A und -6B als Auslöser weiterer Erkrankungen[Bearbeiten | Quelltext bearbeiten]
Die Viren können eine Herzmuskelentzündung bzw. eine Kardiomyopathie auslösen.[5] Außerdem sind sie als mögliche Faktoren bei der Entstehung der Multiplen Sklerose und der Alzheimer-Krankheit[6] in der Diskussion. Eindeutige Daten, die eine Beteiligung an diesen Erkrankungen beweisen würden, gibt es aber nicht. Es existiert eine Studie, die einen Zusammenhang einer HHV-6A-Infektion mit Unfruchtbarkeit nahelegt.[7]
Literatur[Bearbeiten | Quelltext bearbeiten]
- Siegfried Wiersbitzky, Roswitha Bruns, Heidrun Wiersbitzky: Infektionen mit dem Herpesvirus 6 – wirklich nur „Exanthema subitum“? Teil I: Häufigere klinische Krankheitsbilder. In: Fortschritte der Medizin. Band 110, Nr. 32 (S. 41–59), 1992, S. 599–603.
- D. M. Zerr: Human herpesvirus 6: a clinical update. In: Herpes : the journal of the IHMF. Band 13, Nr. 1, Mai 2006, S. 20–24, ISSN 0969-7667. PMID 16732999. (Review).
- L. De Bolle, L. Naesens, E. De Clercq: Update on human herpesvirus 6 biology, clinical features, and therapy. In: Clinical microbiology reviews. Band 18, Nummer 1, Januar 2005, S. 217–245, ISSN 0893-8512. doi:10.1128/CMR.18.1.217-245.2005. PMID 15653828. PMC 544175 (freier Volltext). (Review).
- C. B. Hall, M. T. Caserta u. a.: Chromosomal integration of human herpesvirus 6 is the major mode of congenital human herpesvirus 6 infection. In: Pediatrics. Band 122, Nur. 3, September 2008, S. 513–520, ISSN 1098-4275. doi:10.1542/peds.2007-2838. PMID 18762520.
- G. Morissette, L. Flamand: Herpesviruses and chromosomal integration. In: Journal of virology. Band 84, Nr. 23, Dezember 2010, S. 12100–12109, ISSN 1098-5514. doi:10.1128/JVI.01169-10. PMID 20844040. PMC 2976420 (freier Volltext). (Review).
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e ICTV: ICTV Taxonomy history: Human alphaherpesvirus 1, EC 51, Berlin, Germany, July 2019; Email ratification March 2020 (MSL #35)
- ↑ ICTV: Master Species List 2018b.v2, MSL #34, März 2019
- ↑ S. Z. Salahuddin: Isolation of a new virus, HBLV, in patients with lymphoproliferative disorders. In: Science, Band 234, Nr. 4776, 1986, S. 596–601; PMID 2876520 (englisch).
- ↑ Areej R. El-Jawahri, Pamela W. Schaefer, Joseph B. El Khoury, Maria Martinez-Lage: Case 5-2018: A 63-Year-Old Man with Confusion after Stem-Cell Transplantation. New England Journal of Medicine 2018, Band 378, Ausgabe 7 vom 15. Februar 2018, S. 659–669, DOI: 10.1056/NEJMcpc1707556
- ↑ S. Pankuweit, B. Maisch: Das Herz bei viralen Infektionen. In: Der Internist. Juni 2010, doi:10.1007/s00108-009-2559-8
- ↑ Ben Readhead, Jean-Vianney Haure-Mirande, Cory C. Funk, Matthew A. Richards, Paul Shannon: Multiscale Analysis of Independent Alzheimer’s Cohorts Finds Disruption of Molecular, Genetic, and Clinical Networks by Human Herpesvirus. In: Neuron. Band 0, Nr. 0, Juni 2018, ISSN 0896-6273, doi:10.1016/j.neuron.2018.05.023.
- ↑ R. Marci, V. Gentili, D. Bortolotti, G. Lo Monte, E. Caselli, S. Bolzani u. a.: Presence of HHV-6A in Endometrial Epithelial Cells from Women with Primary Unexplained Infertility. In: PLoS ONE. 11(7), 2016, S. e0158304. doi:10.1371/journal.pone.0158304