Nitrobenzoesäuren
 Van Wikipedia, de gratis encyclopedie
Van Wikipedia, de gratis encyclopedie
Die Nitrobenzoesäuren bilden in der Chemie eine Stoffgruppe, die sich sowohl von der Benzoesäure als auch vom Nitrobenzol ableitet. Die Struktur besteht aus einem Benzolring mit angefügter Carboxy- (–COOH) und Nitrogruppe (–NO2) als Substituenten. Durch deren unterschiedliche Anordnung ergeben sich drei Konstitutionsisomere mit der Summenformel C7H5NO4. Die 4-Nitrobenzoesäure findet vor allem Verwendung in der Analyse organischer Substanzen.
Vertreter[Bearbeiten | Quelltext bearbeiten]
| Nitrobenzoesäuren | ||||||
| Name | 2-Nitrobenzoesäure | 3-Nitrobenzoesäure | 4-Nitrobenzoesäure | |||
| Andere Namen | o-Nitrobenzoesäure | m-Nitrobenzoesäure | p-Nitrobenzoesäure | |||
| Strukturformel |  |  |  | |||
| CAS-Nummer | 552-16-9 | 121-92-6 | 62-23-7 | |||
| PubChem | 11087 | 8497 | 6108 | |||
| Summenformel | C7H5NO4 | |||||
| Molare Masse | 167,12 g·mol−1 | |||||
| Aggregatzustand | fest | |||||
| Kurzbeschreibung | weißes Pulver[1] | gelbliches kristallines Pulver[2] | hellgrünes kristallines Pulver[3] | |||
| Schmelzpunkt | 146–148 °C[1] | 139–142 °C[2] | 239–242 °C[3] | |||
| Siedepunkt | Zers.[1] | Zers.[2] | Zers.[3] | |||
| pKs-Wert | 2,22[4] | 3,44[4] | 3,42[5] | |||
| Löslichkeit in Wasser | 7,8 g/l (25 °C)[1] | 3 g/l (25 °C)[2] | 0,42 g/l (20 °C)[3] | |||
| GHS- Kennzeichnung |
|
|
| |||
| H- und P-Sätze | 315‐319‐335 | 319 | 302‐319 | |||
| keine EUH-Sätze | keine EUH-Sätze | keine EUH-Sätze | ||||
| 280‐302+352‐305+351+338‐304+340‐312 | 264‐280‐305+351+338‐337+313 | 305+351+338 | ||||
Darstellung[Bearbeiten | Quelltext bearbeiten]
3-Nitrobenzoesäure erhält man aus Benzoesäuremethylester durch Umsetzung mit rauchender Salpetersäure in Gegenwart von konzentrierter Schwefelsäure.[6] Nach der Nitrierung wird der entstandene 3-Nitrobenzoesäuremethylester zur Säure verseift.[7]

Wird jedoch die Benzoesäure direkt nitriert, so entsteht zumeist 3,5-Dinitrobenzoesäure.
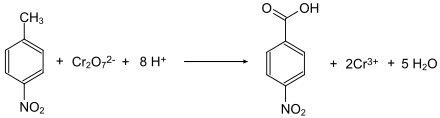
Generell sind die Nitrobenzoesäuren aus den Nitrotoluolen durch Oxidation der Methylgruppe zugänglich. So wird 4-Nitrotoluol mit Natriumdichromat in Gegenwart von konzentrierter Schwefelsäure zur 4-Nitrobenzoesäure oxidiert.[8]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Die Nitrobenzoesäuren sind farblose bis gelbliche kristalline Feststoffe. Die Schmelzpunkte unterscheiden sich deutlich. Die 4-Nitrobenzoesäure, die die höchste Symmetrie aufweist, besitzt den höchsten Schmelzpunkt. Die Nitrobenzoesäuren weisen aufgrund des −M-Effekts der Nitrogruppe eine höhere Acidität im Vergleich zur Benzoesäure auf. Die pKs-Werte sind daher entsprechend niedriger (Benzoesäure: 4,20[4]).
Verwendung[Bearbeiten | Quelltext bearbeiten]
Analytik[Bearbeiten | Quelltext bearbeiten]
Die 4-Nitrobenzoesäure findet vor allem Verwendung in der Analyse organischer Substanzen durch Derivatisierung. Flüssige Substanzen oder solche mit niedrigem Schmelzpunkt werden dazu in leicht kristallisierende Derivate umgewandelt: Alkohole können beispielsweise durch die Messung der Schmelzpunkte ihrer Ester der 4-Nitrobenzoesäure oder der 3,5-Dinitrobenzoesäure identifiziert werden. Hierzu wird die zu analysierende Substanz mit 4-Nitrobenzoesäure in Gegenwart geringer Mengen Schwefelsäure umgesetzt.

4-Nitrobenzoesäure-2-propylester (Smp.: 100,5 °C[4]).
Die Schmelzpunkte dieser Derivate sind in der Regel scharf. Diese Umsetzung ist auch für zahlreiche Amine geeignet.
Die Derivate der 3,5-Dinitrobenzoesäure besitzen in der Regel höhere Schmelzpunkte als die der 4-Nitrobenzoesäure.[4] Sie werden dann bevorzugt gewählt, wenn der Schmelzpunkt mit der 4-Nitrobenzoesäure zu niedrig ist und keine genaue Bestimmung mehr möglich wird.
Ist die fragliche Substanz empfindlicher, so erfolgt stattdessen die direkte Umsetzung mit dem entsprechenden Säurechlorid, dem 4-Nitrobenzoylchlorid. Auf diese Weise sind z. B. auch Derivate der Aminosäuren zugänglich.
Synthese[Bearbeiten | Quelltext bearbeiten]
3-Aminobenzoesäure kann durch die Reduktion von 3-Nitrobenzoesäure erhalten werden. Als Reduktionsmittel eignen sich beispielsweise elementares Zink in Salzsäure[9] oder Hydrazin.[10]
Siehe auch[Bearbeiten | Quelltext bearbeiten]
Weblinks[Bearbeiten | Quelltext bearbeiten]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e Eintrag zu 2-Nitrobenzoesäure in der GESTIS-Stoffdatenbank des IFA, abgerufen am 28. Januar 2024. (JavaScript erforderlich)
- ↑ a b c d e Eintrag zu 3-Nitrobenzoesäure in der GESTIS-Stoffdatenbank des IFA, abgerufen am 28. Januar 2024. (JavaScript erforderlich)
- ↑ a b c d e Eintrag zu 4-Nitrobenzoesäure in der GESTIS-Stoffdatenbank des IFA, abgerufen am 28. Januar 2024. (JavaScript erforderlich)
- ↑ a b c d e CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- ↑ Beyer/Walter: Lehrbuch der Organischen Chemie, 19. Auflage, S. Hirzel Verlag, Stuttgart 1981, ISBN 3-7776-0356-2, S. 511.
- ↑ Oliver Kamm, J. B. Segur: Methyl m-nitrobenzoate In: Organic Syntheses. 3, 1923, S. 71, doi:10.15227/orgsyn.003.0071; Coll. Vol. 1, 1941, S. 372 (PDF).
- ↑ Oliver Kamm, J. B. Segur: m-Nitrobenzoic acid In: Organic Syntheses. 3, 1923, S. 73, doi:10.15227/orgsyn.003.0073; Coll. Vol. 1, 1941, S. 391 (PDF).
- ↑ O. Kamm, A. O. Matthews: p-Nitrobenzoic acid In: Organic Syntheses. 2, 1922, S. 53, doi:10.15227/orgsyn.002.0053; Coll. Vol. 1, 1941, S. 392 (PDF).
- ↑ J. Wilbrand, F. K. Beilstein: Ueber eine neue Reihe isomerer Verbindungen der Benzoëgruppe. – Nitrodracylsäure und deren Derivate, in: J. Liebigs Ann. Chem., 128, 1863, S. 257–273 (doi:10.1002/jlac.18631280302).
- ↑ T. Curtius: Die Einwirkung von Hydrazinhydrat auf Nitroverbindungen. I. Abhandlung, in: J. Prakt. Chem., 76, 1907, S. 233–237 (doi:10.1002/prac.19070760116).
